Tính chất hóa học của khí nitơ
– Các mức oxi hóa mà Nitơ (N) có thể có là: -3, 0, +1, +2, +3, +4, +5.
– Vì phân tử chứa liên kết ba rất bền vững nên ở điều kiện thường, nitơ là một chất ít hoạt động chỉ tham gia phản ứng ở nhiệt độ cao. Nitơ vừa là chất khử vừa là chất oxi hóa.
1. Nitơ là chất oxi hóa
a) Nitơ tác dụng với kim loại → Muối Nitrua.
– PTPƯ: N2 + Kim loại → Muối Nitrua
+ Nhiệt độ thường chỉ tác dụng với Li:
6Li + N2 → 2Li3N
+ Nhiệt độ cao phản ứng với một số kim loại như Mg, Ca và Al,…
2Al + N2 → 2AlN
3Ca + N2 → Ca3N2
b) Nitơ tác dụng với H2 → Amoniac
N2 + 3H2 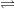 2NH3
2NH3
– Phản ứng này xảy ra trong điều kiện nhiệt độ > 4000C; áp suất p và xúc tác Fe.
2. Nitơ là chất khử (N2 + O2)
– Phản ứng của Nitơ với Oxi xảy ra ở nhiệt độ 30000C hoặc trong lò hồ quang điện
N2 + O2 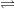 2NO
2NO
– Khí NO không màu hoá nâu trong không khí do phản ứng:
2NO không màu + O2 → 2NO2 (màu nâu đỏ)
Tính chất hóa học cơ bản của photpho
– Các mức oxi hóa có thể có của P: -3, 0, +3, +5.
– P hoạt động hóa học mạnh hơn N2 vì liên kết P – P kém bền hơn so với liên kết N ≡ N.
– P trắng hoạt động hơn P đỏ (vì P trắng có kiểu mạng phân tử còn P đỏ có cấu trúc kiểu polime).
1. Tính oxi hóa của Photpho
– P có phản ứng với nhiều kim loại → muối photphua:
2P + 3Mg → Mg3P2
– Các muối photphua bị thủy phân mạnh giải phóng photphin (PH3).
Ca3P2 + 6H2O → 2PH3 + 3Ca(OH)2
– Photphin là một khí không màu rất độc, có mùi tỏi, bốc cháy trong không khí ở nhiệt độ gần 1500C.
2PH3 + 4O2 → P2O5 + 3H2O
2. Tính khử của Photpho
– Phản ứng với phi kim: O2, halogen,..
4P + 3O2 → 2P2O3
4P + 5O2 → 2P2O5 (nếu O2 dư)
– P trắng phản ứng được ở ngay nhiệt độ thường và có hiện tượng phát quang hóa học; P đỏ chỉ phản ứng khi nhiệt độ > 2500C.
2P + 3Cl2 → 2PCl3
2P + 5Cl2 → 2PCl5
– Phản ứng với các chất oxi hóa khác
6P (đỏ) + 3KClO3 ![xrightarrow[]{t^{0}}](https://hayhochoi.vn/uploads/news/wyswyg/2019_03/1553913037el4ll7q6x8.gif) 3P2O5 + 5KCl (phản ứng xảy ra khi quẹt diêm)
3P2O5 + 5KCl (phản ứng xảy ra khi quẹt diêm)
6P (trắng) + 5K2Cr2O7 → 5K2O + 5Cr2O3 + 3P2O5
P + 5HNO3 → H3PO4 + 5NO2 + H2O
2P + 5H2SO4 đặc → 2H3PO4 + 3H2O + 5SO2
So sánh tính chất hóa học của nitơ và photpho
Tham khảo : https://tailieu.vn/doc/-13-luyen-tap-tinh-chat-cua-nito-photpho-va-cac-hop-chat-cua-chung-1023454.html
Thông tin thêm về n2o
Nitrous Oxide, hay Dinitrogen Oxide, Dinitrogen monoxide, còn gọi là khí gây cười, bóng cười, là hợp chất hóa học ở điều kiện bình thường có dạng khí trong khí quyển Trái Đất, bao gồm 2 nguyên tử Nitơ kết hợp với 1 nguyên tử oxi, công thức là N2O.
Ở nhiệt độ phòng, nó là một khí không màu, không cháy, với một chút kim loại và mùi hương hương vị. Ở nhiệt độ cao, đinitơ monoxit là một chất ôxy hóa mạnh mẽ tương tự như oxy. Nó hòa tan trong nước.
N2O được sinh ra trong quá trình đốt các nhiên liệu hoá thạch. Hàm lượng của nó đang tăng dần trên phạm vi toàn cầu, hàng năm khoảng từ 0,2 – 0,3%. Một lượng nhỏ N2O khác xâm nhập vào khí quyển do kết quả của quá trình nitrat hoá các loại phân bón hữu cơ và vô cơ. N2O xâm nhập vào không khí sẽ không thay đổi dạng trong thời gian dài, chỉ khi đạt tới những tầng trên của khí quyển nó mới tác động một cách chậm chạp với nguyên tử Ôxy.
Trong phòng thí nghiệm, người ta điều chế N2O bằng cách nhiệt phân muối amoni nitrat
Thông tin thêm về n2o4
Đinitơ tetrôxit, là một hợp chất vô cơ có thành phần chính gồm hai nguyên tố nitơ và oxy và có công thức hóa học được quy định là N2O4. Hợp chất này là một thuốc thử hữu ích trong các phản ứng tổng hợp hóa học. Hợp chất này cũng tạo thành một hỗn hợp cân bằng với nitơ dioxit.
Tag: nêu đặc trưng nito n2 nêu sau nào nhất đây ôxi âm
 Công Ty Hóa Chất Hanimex HANIMEX Chemical
Công Ty Hóa Chất Hanimex HANIMEX Chemical