Tính chất hóa học của benzen và đồng đẳng
1. Phản ứng thế của Benzen
a) Thế nguyên tử H của vòng benzen
* Benzen phản ứng với halogen: Benzen + Br2
– Cho benzen và brom vào ống nghiệm khô rồi lắc nhẹ hỗn hợp.
– Cho tiếp một ít bột sắt vào ống nghiệm trên, lắc nhẹ. Màu của brom nhạt dần và thấy có khí hiđro bromua thoát ra do đã xảy ra phản ứng thế: 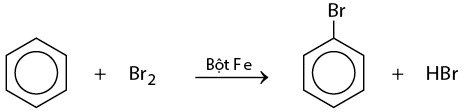
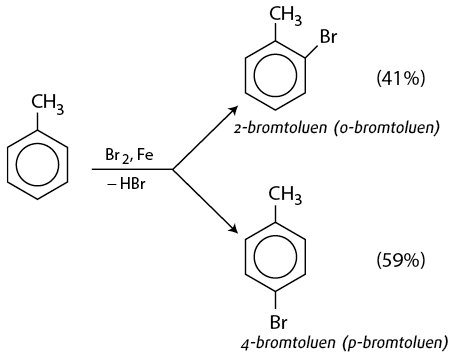
– Nếu cho các ankylbenzen phản ứng với brom trong điều kiện có bột sắt sẽ thu được hỗn hợp sản phẩm thế brom chủ yếu vào vị trí para và ortho so với nhóm ankyl:
* Benzen phản ứng với axit nitric: Benzen + HNO3
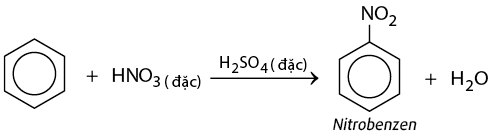
– Cho benzen vào ống nghiệm chứa sẵn hỗn hợp H2SO4 đặc và HNO3 đặc. Khi đó sẽ thấy có lớp chất lỏng nặng màu vàng nhạt lắng xuống. Đó là nitrobenzen được tạo thành theo phản ứng sau:
 * Quy tắc thế: Các ankylbenzen dễ tham gia phản ứng thế nguyên tử H của vòng benzen hơn benzen và sự thế ưu tiên ở vị trí ortho và para so với nhóm ankyl.
* Quy tắc thế: Các ankylbenzen dễ tham gia phản ứng thế nguyên tử H của vòng benzen hơn benzen và sự thế ưu tiên ở vị trí ortho và para so với nhóm ankyl.
b) Thế nguyên tử H của mạch nhánh
– Nếu đun toluen hoặc các ankylbenzen với brom, sẽ xảy ra phản ứng thế nguyên tử H của mạch nhánh tương tự ankan.
– Ví dụ, phản ứng của Toluen với Brom tạo Benzyl bromua: 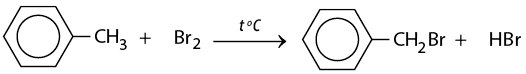
2. Phản ứn cộng của Benzen
a) Benzen phản ứng cộng hiđro: Benzen + H2
C6H6 + 3H2 ![small xrightarrow[]{t^{0},Ni}](https://hayhochoi.vn/uploads/news/wyswyg/2019_04/1555557081ohm0n74n7l.gif) C6H12 (xiclohexan)
C6H12 (xiclohexan)
b) Benzen phản ứng cộng clo: Benzen + Cl2
– Dẫn lượng nhỏ khí clo vào bình chứa một ít benzen, đậy kín lại rồi đưa bình ra ngoài ánh nắng. Trong bình xuất hiện khói trắng và thành bình xuất hiện một lớp bột màu trắng, đó là 1,2,3,4,5,6-hexa clo xiclohexan (hexacloran).
C6H6 + 3Cl2 ![small xrightarrow[]{as'}](https://hayhochoi.vn/uploads/news/wyswyg/2019_04/1555557084ld2we8spxc.gif) C6H6Cl6 (hexacloran)
C6H6Cl6 (hexacloran)
3. Phản ứng oxi hoá benzen và đồng đẳng
a) Phản ứng oxi hoá không hoàn toàn của benzen và đồng đẳng
– Thí nghiệm:
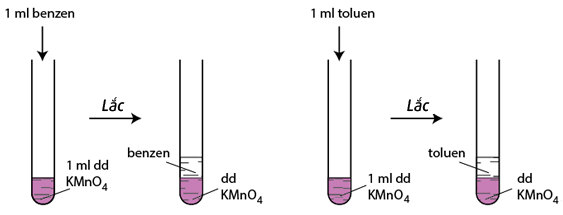
Benzen và Toluen không làm mất màu dung dịch KMnO4 ở điều kiện thường
– Khi đun nóng đồng thời cả hai ống nghiệm trong nồi cách thuỷ:
+ Benzen vẫn không làm mất màu dung dịch kali pemanganat KMnO4.
+ Toluen làm mất màu dung dịch kali pemanganat, tạo kết tủa mangan đioxit.
C6H5-CH3 (toluen) + KMnO4 ![small xrightarrow[]{t^{0}}](https://hayhochoi.vn/uploads/news/wyswyg/2019_04/15555570884rzrkn6wy8.gif) C6H5-COOK (kali benzoat) + 2MnO2↓ + KOH + H2O
C6H5-COOK (kali benzoat) + 2MnO2↓ + KOH + H2O
b) Phản ứng oxi hoá hoàn toàn benzen và đồng đẳng
– Các hiđrocacbon thơm khi cháy toả nhiều nhiệt như PTTQ sau:
CnH2n-6 + [(3n-3)/2]O2 ![small xrightarrow[]{t^{0}}](https://hayhochoi.vn/uploads/news/wyswyg/2019_04/15555570884rzrkn6wy8.gif) nCO2 + (n-3)H2O
nCO2 + (n-3)H2O
B. MỘT SỐ HIĐROCACBON THƠM KHÁC
I. STIREN (VinylBenzen)
1. Cấu tạo và tính chất vật lí của Stiren
a) Cấu tạo của Stiren
– Công thức phân tử:C8H8
– Công thức cấu tạo của Stiren:
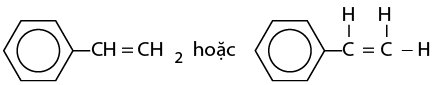
công thức cấu tạo của stiren (vinylbenzen)
b) Tính chất vật lý của Stiren (vinyl benzen)
– Stiren còn gọi là vinylbenzen là chất lỏng không màu, sôi ở 1460C, tan nhiều trong dung môi hữu cơ.
2. Tính chất hoá học của Stiren
a) Stiren phản ứng với dung dịch brom
C6H5-CH=CH2 + Br2 (dd) → C6H5-CHBr-CH2Br
b) Stiren phản ứng với hiđro
– Khi cho stiren tác dụng với hiđro dư có xúc tác ở nhiệt độ và áp suất cao sẽ thu được etylxiclohexan:
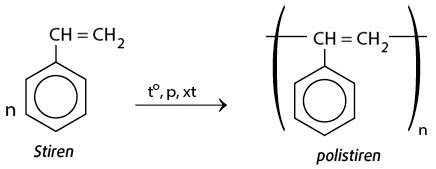
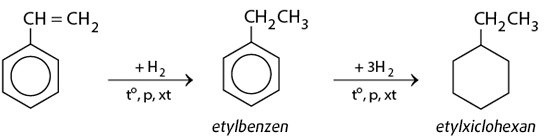 c) Stiren phản ứng trùng hợp
c) Stiren phản ứng trùng hợp
 II. NAPHTALEN
II. NAPHTALEN
1. Cấu tạo và tính chất vật lí Naphtalen
a) Cấu tạo của Naphtalen
– Công thức phân tử: C10H8
– Công thức cấu tạo của naphtalen:
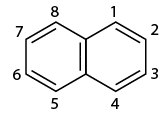
b) Tính chất vật lý của Naphtalen
– Naphtalen (băng phiến) là chất rắn, nóng chảy ở 800C, tan trong benzen, ete,… và có tính thăng hoa.
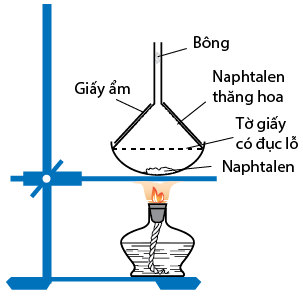 2. Tính chất hoá học của Naphtalen
2. Tính chất hoá học của Naphtalen
a) Phản ứng thế của naphtalen
– Naphtalen tham gia phản ứng thế tương tự benzen, nhưng phản ứng xảy ra dễ dàng hơn và thường ưu tiên thế vào vị trí số 1.
• Naphtalen + Br2
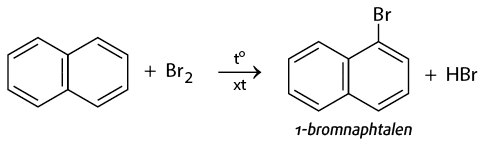 • Naphtalen + HNO3
• Naphtalen + HNO3
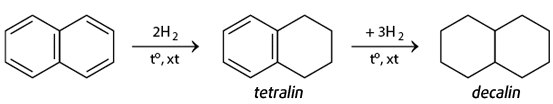
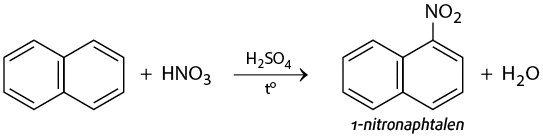 b) Phản ứng cộng hidro của naphtalen
b) Phản ứng cộng hidro của naphtalen
– Khi có chất xúc tác, naphtalen cộng hiđro tạo ra đecalin:
Tính chất hóa học của metan etilen axetilen benzen
• Điểm giống nhau giữa Etilen và Axetilen
– Đều là các hidrocacbon trong phân tử có C và H
– Trong phân tử có liên kết σ bền và liên kết π linh động
– Liên kết π linh động dễ bị đứt (bẻ gãy) khi tham gia phản ứng hóa học
– Tính chất hóa học đặc trưng là phản ứng cộng, ngoài ra có phản ứng trùng hợp và oxi hóa.
• Điểm khác nhau giữa Etilen và Axetilen
– Tùy điều kiện và xúc tác mà khi tham gia phản ứng 1 hay 2 liên kết π của Axetilen bị đứt.
– Axetilen có 2 nguyên tử H linh động có thể tham gia phản ứng thế với ion kim loại.
• Điểm giống nhau giữa Axetilen và Benzen
– Đều là các hidrocacbon trong phân tử có C và H (C2H2 mạch thẳng, C6H6 mạch vòng).
– Trong phân tử có liên kết σ bền và liên kết π linh động.
– Cùng có phản ứng đặc trưng là phản ứng cộng.
• Điểm khác nhau giữa Axetilen và Benzen
– Với Axetilen tùy điều kiện và xúc tác mà khi tham gia phản ứng 1 hay 2 liên kết π của Axetilen bị đứt. Ngoài ra Axetilen có phản ứng trùng hợp và oxi hóa.
– Với Benzen cấu tạo mạnh vòng, có 3 liên kết π liên hợp với nhau tạo thành hệ thơm bền vững nên có tham gia phản ứng cộng nhưng khó (chỉ cộng H2), dễ tham gia phản ứng thế và bền với tác nhân oxi hóa.
– Axetilen có 2 nguyên tử H linh động có thể tham gia phản ứng thế với ion kim loại.
So sánh tính chất hóa học của etylbenzen với stiren
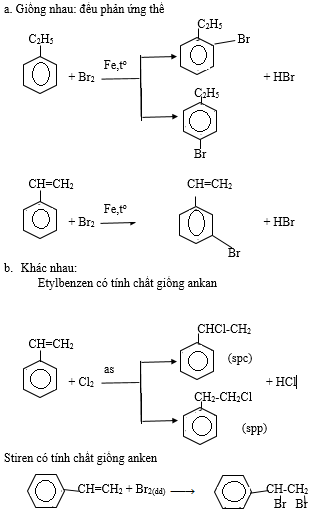
Tag: 11 nêu trình bày
 Công Ty Hóa Chất Hanimex HANIMEX Chemical
Công Ty Hóa Chất Hanimex HANIMEX Chemical