Na2co3 là chất gì
Natri cacbonat, còn gọi là soda, là một loại muối cacbonat của natri có công thức hóa học là Na2CO3. Na2CO3 có nhiều trong tự nhiên như nước khoáng, nước biển, tro của rong biển và muối mỏ trong lòng đất. Na2CO3 khan tồn tại ở dạng bột màu trắng, dễ hút ẩm, nóng chảy ở nhiệt độ 851 độ C. Dễ tan trong nước, khi tan tỏa ra nhiều nhiệt.
Viết công thức cấu tạo của na2co3
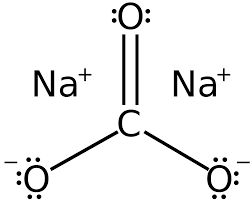
Tính chất vật lý
– Natri cacbonat tồn tại ở dạng chất rắn khan, không mùi, màu trắng và là một chất hút ẩm tốt.
Natri cacbonat dạng tinh thể màu trắng
– Khối lượng riêng: 2.532 g/cm3, thể rắn
– Khối lượng mol: 105.9884 g/mol
– Nhiệt độ nóng chảy: 851oC (1124 K)
– Nhiệt độ sôi: 1600 °C (2451 K)
– Nhiệt độ phân hủy: 853oC
– Độ tan: Tan hoàn toàn trong nước nóng, glycerol, axit sunfuic . Ở 20°C, độ tan trong nước là 22 g/100 ml, phản ứng tỏa nhiệt lớn. Hòa tan một phần trong dung dịch acetone, alcohol, methanol.
– Trạng thái dung dịch
+ Thấp hơn 32.5°C: Kết tinh thành Na2CO3.10H2O
+ Từ 32.5 – 37.5°C: Tạo thành tạo Na2CO3.7H2O
+ Từ 37.5°C đến dưới 107°C: Biến đổi thành Na2CO3.H2O
+ Từ 107°C: Trở thành natri cacbonat khan do nước hoàn toàn bị bốc hơi hết.
– Hidrat được tạo thành do hòa tan natri cacbonat trong nước có độ tan thay đổi theo nhiệt độ, nhiệt độ càng cao thì độ tan càng lớn trong khi điều nay lại ngược lại hoàn toàn với monohidrat.
– Trong không khí, decahiđrat Na2CO3.10H2O dễ xảy ra hiện tượng thoát nước để trở thành dạng bột có màu trắng Na2CO3.5H2O.
– Tính ăn mòn: Không ăn mòn thủy tinh nhưng dung dịch natri cacbonat đặc nóng có thể ăn mòn thép.
Tính chất hóa học
Cấu trúc hóa học Natri cacbonat

– Làm thay đổi màu sắc chất chỉ thị khi bị thủy phân trong nước do tạo ra dung dịch Na2CO3 có tính bazơ yếu.
+ Dung dịch phenolphtalein không màu chuyển sang màu hồng.
+ Quỳ tím chuyển sang màu xanh.
Na2CO3 → 2Na+ + CO32−
CO32− + H2O ↔ HCO3− + OH−
– Tác dụng với axit mạn, sủi bọt, tạo thành muối, nước và khí cacbonic
Na2CO3 + 2HCl → 2NaCl + H2O + CO2
– Tác dụng với muối tạo thành hai muối mới
Na2CO3 + CaCl2 → 2NaCl + CaCO3
– Tác dụng với CO2 và nước xảy ra phản ứng thuận nghịch
Na2CO3 + CO2 + H2O ↔ 2NaHCO3
– Tác dụng mạnh với F2, lithium, 2,4,6- trinitrotoluene.
– Không tương thích với phosphorus peritoxit, fluoride, amonia + bạc nitrat, 2,4,6- trinitrotoluence, amonia, axit, natri sunfat + nước, hydrogen proxit, nhôm (gây nổ nếu nhôm đang nóng đỏ), natri sunfat, zic, canxi hidroxit, natri cacbonat + amonia (tạo thành dung dịch arabic gum gây nổ).
– Na2CO3 mang tính bazo.
CO3 2- + H2O -> HCO3- + OH-
– Có thể làm mềm nước cứng toàn phần bằng dung dịch Na2CO3
Na2CO3 có kết tủa không?
Na2CO3 là một chất không kết tủa. Ở điều kiện thường, Na2CO3 ở dạng bột có màu trắng, mùi nồng. Khi để lâu ngoài không khó sẽ có hiện tượng chảy nước. Tuy nhiên, khi phản ứng với một số chất, Na2CO3 có thể tạo ra kết tủa. Để hiểu hơn về phần kiến thức này, chúng ta hãy cùng tìm hiểu kỹ hơn về tính chất vật lý và hóa học của nó nhé
Na2CO3 có ứng dụng gì
#3: na2co3 là nguyên liệu chính dùng trong y học công nghệ thực phẩm chế tạo nước giải khát
#4: na2co3 dùng để tẩy sạch vết dầu mỡ bám trên chi tiết máy trước khi sơn
Ôn tập bài tập Na2CO3
Bài tập 1: Na2co3 có phải là hợp chất hữu cơ không
Chất không phải chất hữu cơ là Na2CO3
Bài tập 2: Dung dịch Na2CO3 tác dụng được với dung dịch nào sau đây ?
| A. | KNO3. |
| B. | CaCl2. |
| C. | Na2SO4. |
| D. | KOH. |
Đáp án B
Tag: j bền môi trường lưỡng kno3 ngậm đun x dd tên hay xh2o ko k liên tạm thời
 Công Ty Hóa Chất Hanimex HANIMEX Chemical
Công Ty Hóa Chất Hanimex HANIMEX Chemical