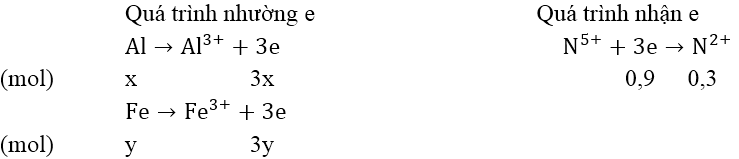Bài 1: bài tập tính ph của dung dịch axit yếu
Hoà tan 1,07g NH4Cl vào nước được 2 lít dung dịch X.
a. Tính pH của dung dịch X biết hằng số phân li bazơ của NH3 là 1,8.10-5.
b. Nếu thêm vào dung dịch X 100 ml dd HCl 0,01M được dd Y. Tính pH của dd Y?
Trả lời
a. nNH4Cl = 1,07/53,5 = 0,02 => CM(NH4Cl) = 0,02/2 = 0,01 M
Phương trình điện li:
NH4Cl → NH4+ + Cl–
NH4+ + H2O ⇌ NH3 + H3O+
Ban đầu 0,01
Điện ly: x x x
Sau điện li: 0,01-x x x
Kb = x2/(0,01-x) = 1,8.10-5 => x = 4,24.10-4 => pH = 3,37
b. Phương trình điện li:
HCl → H+ + Cl+
NH4+ + H2O ⇌ NH3 + H3O+
Ban đầu 0,01 0,001
Điện ly x x x
Sau điện li: 0,01-x x x+0,001
Kb = (x.(x+0,001))/(0,01-x) = 1,8.10-5 => x = 3,69.10-4 => pH = 3,43
2. Bài tập kim loại tác dụng với dung dịch axit
Cho 11 gam hỗn hợp Al và Fe vào dung dịch HNO3 loãng lấy dư thì có 6,72 lít khí NO bay ra (đktc). Tính khối lượng của mỗi kim loại trong hỗn hợp.
Hướng dẫn:
Gọi số mol Al và Fe trong hỗn hợp là x, y (mol)
Bảo toàn electron: 3x + 3y = 0,9 ⇒ x + y = 0,3 (1)
mhỗn hợp = 27x + 56y = 11 (2)
Giải hệ phương trình (1) và (2): x = 0,2 (mol); y = 0,1 (mol)
Vậy mAl = 5,4 (gam) và mFe = 5,6 (gam)
Bài 3: ba dung dịch axit đậm đặc hcl h2so4 hno3
Ba dung dịch axit đậm đặc HCl, H2SO4, HNO3 đựng trong ba lọ bị mất nhãn. Nêu chỉ chọn một chất làm thuốc thử để nhận biết ba dung dịch axit trên, ta có thể dùng:
| A. | Cu |
| B. | CuO |
| C. | CaCO3 |
| D. | Ba(OH)2 |
Lời giải: Đáp án A
CuO tan trong cả 3 dd axit trên nhưng không có hiện tượng gì.
Dùng CaCO3 thì cả 3 cùng có sủi bọt khí CO2.
Dùng Ba(OH)2 thì chỉ nhận biết được H2SO4 (tạo kết tủa tắng).
Vậy chọn A.Cu khi cho vào 3 dung dịch axit nhạn biết được như sau:
Lọ không xảy ra hiện tượng là HCl
Lọ có khí không màu thoát ra(SO2) là H2SO4
Lọ có khí không màu thoát ra ( NO ) hoá nâu trong không khí là HNO3
Ta thấy HCl nhận ra vì ko có pư tạo khí và Cu rắn sẽ lắng xuống
2 axit còn lại tạo muối CuSO4,CuNO3
làm khô 2 muối thì CuSO4 từ xanh -> trắng (CuSO4 khan) => chọn Cu
Bài 4: bỏ quả trứng vào dung dịch axit clohiđric
Bỏ quả trứng vào dung dịch axit clohiđric thấy sủi bọt ở vỏ trứng (hình bên).
Biết rằng axit clohiđric đã tác dụng với canxi cacbonat (chất có trong vỏ trứng) tạo ra canxi clorua, nước và khí cacbon đioxit thoát ra.
Hãy chỉ ra dấu hiệu để nhận biết có phản ứng xảy ra. Ghi lại phương trình chữ của phản ứng.
Lời giải:
Dấu hiệu để nhận biết phản ứng xảy ra là vỏ trứng sủi bọt, do khí cacbon đioxit thoát ra ngoài.
Phương trình chữ của phản ứng:
Axit clohiđric + canxi cacbonat → canxi clorua + cacbon đioxit + nước
Chất phản ứng: axit clohiđric và canxi cacbonat.
Sản phẩm: canxi clorua, khí cacbon đioxit, nước.
Bài 5: hòa tan 16.8 gam fe trong dung dịch axit hno3
Hoà tan 16,8 gam Fe trong dung dịch axit HNO3 (đặc, nóng, dư). Sau khi phản ứng xảy ra hoàn toàn, thu được V lít khí NO (sản phẩm khử duy nhất, đktc). Giá trị của V là
A. 6,72
B. 10,08
C. 11,20
D. 13,44
Lời giải
Chọn A
nFe = 16,8/56 = 0,3 mà HNO3 dư Þ Tạo Fe3+
BTE Þ nNO = 0,3×3/3 = 0,3 Þ V = 0,3×22,4 = 6,72
Bài 6: cho 200ml dung dịch axit photphoric
| A. | 39,225 gam. |
| B. | 35,225 gam. |
| C. | 41,225 gam. |
| D. | 10,1 gam. |
Lời giải:

Bài 7: đun nóng xenlulozơ trong dung dịch axit
Đun nóng xenlulozơ trong dung dịch axit vô cơ, thu được sản phẩm là
Cho 200ml dung dịch X chứa axit HCl 1M và NaCl 1M. Số mol của các ion Na+, Cl–, H+ trong dung dịch X lần lượt là:
| A. | 0,2; 0,2; 0,2. |
| B. | 0,1; 0,2; 0,1. |
| C. | 0,2; 0,4; 0,2. |
| D. | 0,1; 0,4; 0,1. |
HCl → H+ + Cl–
0,2——0,2——–0,2
NaCl → Na+ + Cl–
0,2——0,2——–0,2
→ nNa+ = 0,2 mol; nCl– = 0,2 + 0,2 = 0,4 mol; nH+ = 0,2 mol
→ Chọn C.
Bài 8: dung dịch x chứa hỗn hợp 2 axit hcl 0.4m
Dung dịch X chứa hỗn hợp 2 aĩt HCl 0.4M và H2SO4 0.1M. Dung dịch Y chứa hh 2 hidroxit KOH 0.1M và Ba(OH)2 0.2M. Tính thể tích dung dịch Y cần dùng để trung hòa 200ml dung dịch X và khối lượng kết tủa thu đc.
n HCl = 0.4 .0.2 = 0.08 (mol)
viết PTPhân ly
suy ra n H+ = 0.08 (mol)
n H2SO4 = 0.1 .0.2 = 0.02 (mol)
viết PTPhân ly
suy ra n H+ = 0.04 (mol)
n H+ (tổng công) = 0.12 (mol)
gọi V là thể tích hh bazo cần tìm
n Ba(OH)2 = 0.2 V (mol)
suy ra n OH- = 0.4 V (mol)
n KOH = 0.1 V suy ra n OH- = 0.1 V (mol)
n OH- (tổng cộng) = 0.5 V
VẬY n H+ = n OH-
SUY RA 0.12 = 0.5V
suy ra V = 0.24 (l)
n Ba2+ = 0.2V = 0.048 (mol)
n SO4 2- = 0.02 (mol)
suy ra so mol ket tua keo theo SO4 2- = 0.02 mol
Ba 2+ + SO4 2- = BaSO4
…………..0.02………0.02
m BaSO4 = 0.02 . 233 = 4.66 (g)
Bài 9: đối với dung dịch axit yếu ch3cooh 0 1m
Đối với dung dịch axit yếu CH3COOH 0,1M, nếu bỏ qua sự điện li của nước thì đánh giá nào về nồng độ mol ion nào sau đây là đúng?
| A. | [H+] = 0,1M. |
| B. | [H<súp>+</súp>] < 0,1M. |
| C. | [H+] < [CH3COO–]. |
| D. | [H+] > [CH3COO–]. |
Lời giải:
CH3COOH là chất điện li yếu: CH3COOH ⇄ CH3COO– + H+
⇒ [H+] = [CH3COO–] = [CH3COOH]điện li < [CH3COOH]ban đầu = 0,1M
⇒ chọn B.
Bài 10: Dung dịch axit axetic 0,60,6% có khối lượng riêng xấp xỉ 11g/ml. Độ điện li của axit axetic trong điều kiện này là 1,01,0%. Tính nồng độ mol của ion H+H+ trong dung dịch đó (bỏ qua sự điện li của nước).
Lời giải:
Một lít dung dịch (1000ml)(1000ml) có khối lượng là 1000g1000g.
Khối lượng axit axetic trong 1000g1000g dung dịch đó là: 1000.0,6100=6(g)1000.0,6100=6(g).
Số mol axit axetic trong 11lít dung dịch là: 660=0,1660=0,1(mol).
Như vậy, dung dịch có nồng độ axit là 0,10,1 mol/l.
CH3COOHH⇆++CH3COO−CH3COOHH⇆++CH3COO−
Số mol axit axetic đã phân li: 0,1.1100=0,0010,1.1100=0,001(mol).
Số mol H+H+ cũng là 0,0010,001. Nồng độ H+H+ là 0,0010,001 mol/l hay 10−310−3 mol/l.
Tag: giấm ăn những phần tử glucozo glixerol etanol toán pha loãng bán sunfuric cách bao nhiêu dẫn dãy phenylamoni 10ml ph=3 kẽm naoh so2 sunfuhidric dạng in english trái tim em hai tấm ngâm h3po4 muốn mol/l protein hoặc kiềm sinh tăng 98 saccarozo thổ ph=5 phải thế ph=2 ph=4 cốc đựng clohidric lá sắt nhôm nhỏ vài giọt đá vôi giữa chế quỳ tím chuyển thành sang ắc quy khác nhau sục sunfuro nitric 63 trăm acquy chì hno2 tinh bột 10m hx công thức khoảng xenlulozo đổ 2ml 100ml 6g 25 trộn 30 300ml 50ml 67 94 bình thủy sao khiết lâu mg mgo oh sio2 hf hbr hi đồng thời môi trường dưới da cam thử nấc gồm đa đệm acrylic tất cuoh2 boric 03m citric flohidric hyaluronic kể h cộng trừ h2 hóa học ánh sáng oxi nghĩa giống điểm salicylic tiếng anh xitric 1ml nitrơ hclo 20g đơn chức 23 hồng phenolphtalein brom 20
 Công Ty Hóa Chất Hanimex HANIMEX Chemical
Công Ty Hóa Chất Hanimex HANIMEX Chemical