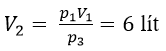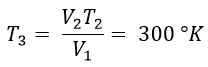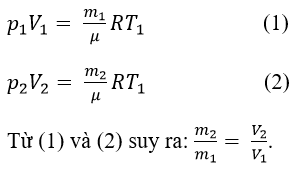Tỉ khối của chất khí
• Khái niệm tỉ khối của chất khí:
– Tỉ khối là khái niệm chỉ sử dụng cho chất khí.
– Để biết khí A nặng hay nhẹ hơn khí B bao nhiêu lần, ta so sánh khối lượng mol của khí A (MA) với khối lượng mol của khí B (MB).
• Công thức tính tỉ khối của chất khí: 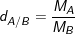
– Trong đó: 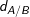 : tỉ khối của khí A đối với khí B
: tỉ khối của khí A đối với khí B
MA: khối lượng mol của khí A
MB: khối lượng mol của khí B
– Tỉ khối là công thức xác định phân tử khối của chất khí A so với chất khí B xem chất A nặng hay nhẹ hơn chất B bao nhiêu lần.
Sự nở vì nhiệt của chất khí
- Cắm một ống thủy tinh nhỏ xuyên qua nút bình cầu
- Cho một giọt nước màu vào trong ống thuỷ tinh.
- Lắp chặt nút cao su có ống thủy tinh chứa nước màu vào bình cầu.
- Xát hai lòng bàn tay vào nhau cho nóng lên, sau đó áp chặt vào bình cầu
.PNG)
- Có hiện tượng gì xảy ra với giọt nước trong ống thủy tinh? Hiện tượng này chứng tỏ thể tích không khí trong bình cầu thay đổi thế nào?
- Ta thấy giọt nước màu đi lên, chứng tỏ thể tích khí trong bình nở ra.
- Nói cách khác: đã có lực tác dụng vào giọt nước đẩy giọt nước đi lên, lực này do không khí dãn nở mà có
- Khi ta thôi không áp tay vào bình cầu, có hiện tượng gì xảy ra với giọt nước màu trong ống thủy tinh? Hiện tượng này chứng tỏ điều gì?
- Giọt nước màu đi xuống, chứng tỏ thể tích không khí trong bình giảm, không khí trong bình co lại
- Tại sao thể tích không khí trong bình cầu lại tăng khi ta áp hai bàn tay nóng vào bình?
- Thể tích khí trong bình tăng lên là do không khí trong bình nóng lên
- Tại sao thể tích không khí trong bình cầu lại giảm khi ta thôi không áp hai bàn tay nóng vào bình?
- Thể tích khí trong bình giảm đi là do không khí trong bình lạnh đi.
Bảng 1: So sánh sự nở vì nhiệt của các chất rắn, lỏng và khí.
| Chất khí | Chất lỏng | Chất rắn |
| Không khí : 183cm3 | Rượu : 58cm3 | Nhôm : 3,54cm3 |
| Hơi nước : 183cm3 | Dầu hỏa : 55 cm3 | Đồng : 3,55cm3 |
| Khí oxy : 183cm3 | Thủy ngân : 9 cm3 | Sắt : 1,80 cm3 |
- Các chất khí khác nhau nhưng lại nở vì nhiệt giống nhau.
- Chất khí nở vì nhiệt nhiều hơn chất lỏng, chất lỏng nở vì nhiệt nhiều hơn chất rắn.
a. Thể tích khí trong bình tăng khi nóng lên.
b. Thể tích khí trong bình giảm khi lạnh đi.
c. Chất rắn nở ra vì nhiệt ít nhất, chất khí nở ra vì nhiệt nhiều nhất.
- Vậy:
- Chất khí nở ra khi nóng lên, co lại khi lạnh đi.
- Các chất khí khác nhau nở vì nhiệt giống nhau.
- Chất khi nở vì nhiệt nhiều hơn chất lỏng, chất lỏng nở vì nhiệt nhiều hơn chất rắn
Dòng điện trong chất khí
• Quá trình phóng điện tự lực trong chất khí là quá trình phóng điện vẫn tiếp tục giữ được khi không còn tác nhân ion hóa tác động từ bên ngoài.
• Có bốn cách chính để dòng điện có thể tạo ra hạt tải điện mới trong chất khí:
1. Dòng điện qua chất khí làm nhiệt độ khí tăng rất cao, khiến phân tử khí bị ion hoá
2. Điện trường trong chất khí rất lớn, khiến phân tử khí bị ion hoá ngay khi nhiệt độ thấp.
3. Catôt bị dòng điện nung nóng đỏ, làm cho nó có khả năng phát ra electron. Hiện tượng này gọi là hiện tượng phát xạ nhiệt electron
4. Catôt không nóng đỏ nhưng bị các ion dương có năng lượng lớn đập vào làm bật electron khỏi catôt trở thành hạt tải điện
– Hai kiểu phóng điện tự lực thường gặp nhất là Tia lửa điện và Hồ quang điện.
Cách nhận biết các chất khí
|
Chất cần nhận biết |
Thuốc thử |
Hiện tượng |
Phương trình phản ứng |
|
I2 (hơi) |
Hồ tinh bột |
Không màu→xanh |
|
|
Cl2 |
Nước Br2 (màu nâu) |
Nhạt màu |
5Cl2 + Br2 + 6H2O → 10HCl + 2HBrO3 |
|
dd KI + hồ tinh bột |
Không màu→xanh |
|
|
|
O2 |
Tàn đỏ que đóm |
Bùng cháy |
|
|
Cu (đỏ), t0 |
Hóa đen |
2Cu + O2 → CuO |
|
|
H2 |
Đốt, làm lạnh |
Hơi nước đọng lại |
2H2 + O2 → 2H2O |
|
CuO (đen), t0 |
Hóa đỏ (Cu) |
CuO + H2 → Cu + H2O |
|
|
H2O (hơi) |
CuSO4 khan |
Màu trắng→xanh |
CuSO4 + 5H2O → CuSO4.5H2O |
|
CO |
dd PdCl2 |
Pd↓ vàng |
CO + PdCl2 + H2O → Pd↓ + 2HCl + CO2 |
|
CuO (đen), t0 |
Hóa đỏ (Cu) |
CuO + CO → Cu + CO2 |
|
|
CO2 |
dd nước vôi trong |
↓ vẩn đục trắng |
CO2 + Ca(OH)2 → CaCO3↓ + H2O |
|
SO2 |
Nước Br2 (màu nâu) |
Nhạt màu |
SO2 + Br2 + 2H2O → H2SO4 + 2HBr |
|
dd thuốc tím |
Nhạt màu |
5SO2 + 2 KMnO4 + 2H2O → 2H2SO4 + 2MnSO4 + K2SO4 |
|
|
SO3 |
dd BaCl2 |
↓ trắng |
BaCl2 + SO3 + H2O → BaSO4↓ + 2HCl |
|
H2S |
Khứu giác |
Mùi trứng thối |
|
|
dd Pb(NO3)2 |
↓ đen |
Pb2+ + H2S → PbS↓ + 2H+ |
|
|
HCl |
Quỳ tím ẩm |
Hóa đỏ |
|
|
NH3 |
Tạo khói trắng |
HCl + NH3 → NH4Cl |
|
|
dd AgNO3 |
↓ trắng |
HCl + AgNO3 → AgCl↓ + HNO3 |
|
|
NH3 |
Quỳ tím ẩm |
Hóa xanh |
|
|
HCl (đặc) |
Tạo khói trắng |
NH3 + HCl → NH4Cl |
|
|
Khứu giác |
Mùi khai |
|
|
|
NO |
Không khí |
Hóa nâu |
2NO + O2 → 2NO2 |
|
NO2 |
Thị giác |
Màu nâu |
|
|
Quỳ tím ẩm |
Hóa đỏ |
3NO2 + H2O → 2HNO3 + NO |
|
|
Làm lạnh |
Màu nâu→Ko màu |
2NO2 → N2O4 |
|
|
N2 |
Que đóm cháy |
Tắt |
|
|
Sinh vật nhỏ (dế, thằn lằn,…) |
Chết |
|
Bài tập đồ thị biến đổi trạng thái của chất khí
A. Phương pháp & Ví dụ
Lý thuyết – Phương pháp giải
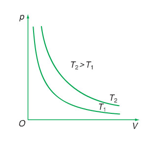
– Đường đẳng nhiệt:
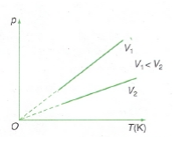
– Đường đẳng tích:
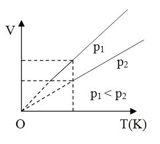
– Đường đẳng áp:
Bài tập vận dụng
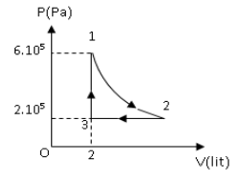
Bài 1: Một khối khí thực hiện 1 chu trình như hình vẽ. Cho p1 =6.105 Pa, V1 = 2 lít, T2 = 100°K, p3 = 2.105 Pa.
a. Nêu tên gọi các đẳng quấ trình trong chu trình. Tính V2 và T3.
b. Vẽ lại chu trình trên trong hệ tọa độ (p,T).
Hướng dẫn:
a. (1) ⇒ (2): đẳng nhiệt.
(2) ⇒ (3): đẳng áp.
(3) ⇒ (1): đẳng tích.
Từ các đẳng quá trình ta suy ra: T1 = T2, p2 = p3, V3 = V1.
Từ quá trình đẳng nhiệt ta có:
p1.V1 = p2.V2 ⇔ p1.V1 = p3.V2 ⇔
Từ quá trính đẳng áp ta có:
V3.T3 = V2.T2 ⇔ V1.T3 = V2. T2 ⇔
b. Vẽ đồ thị.
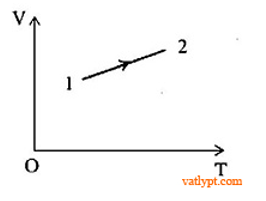
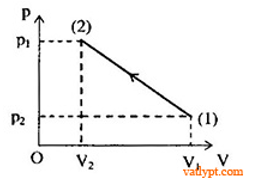
Bài 2: Một xilanh chưa khí bị hở nên khí có thể ra vào nhanh hoặc chậm. Khí áp suất p không đổi, thể tích V biến thiên theo nhiệt độ tuyệt đối T như đồ thị. Hỏi lượng khí trong xilanh tăng hay giảm?
Hướng dẫn:
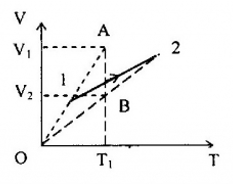
Vẽ đường thẳng qua T1, song song với trục OV, cắt đồ thị (V, T) của hai khí tại A ( p1, V1, T1) và B ( p1, V2, T1):
Vì V2 < V1 nên m2 < m1: khối lượng khí trong bình giảm.
Bài 3: Có 20g khí Heli chứa trong xilanh đậy kín bởi 1 pittong biến đổi chậm từ (1) đến (2) theo đồ thị như hình vẽ. Cho V1 = 30 lít, p1 = 5 atm, V2 = 10 lít, p2 = 15 atm. Tìm nhiệt độ cao nhất mà khí đạt được trong quá trình trên.
Hướng dẫn:
Quá trình từ (1) đến (2): p = aV + b.
Thay các giá trị (p1, V1) và (p2, V2) vào ta được:
5 = 30a + b (1)
10 = 10a + b (2)
Từ (1) và (2) suy ra:
Tag: bản hợp hidro nguyên tố rh4 rh3 dẫn kiện trắc chương violet powerpoint đáp án về tiêu chuẩn giảng ôn dùng naoh ở khô dạng lớp ankan clo xuất monoclo đề kiểm tra học phần trăm r laser 11 môi nào đây chữa sản đau dạ dày chuyển dời tỷ số dung muốn đun phải phía dưới giáo mất brom vôi dựa oxit hiđro riêng 20 sách tan luật thiết giới những dễ nén cơ tiết nâng x dịch trung đktc 8 propylamin cấu gây hiệu nhà kính sơ tư duy
 Công Ty Hóa Chất Hanimex HANIMEX Chemical
Công Ty Hóa Chất Hanimex HANIMEX Chemical
.PNG)