Tìm Hiểu Tính Chất Hóa Học Của Axit HCl
HCl hay Axit clohydric là một trong những chất hóa học có nhiều ứng dụng rộng rãi đóng vai trò quan trọng trong nhiều lĩnh vực công nghiệp . Hôm nay Hanimex xin được thông tin thêm đến bạn đọc một vài điều cần biết về tình chất hóa học của hcl nhé.
Axit clohiđric là axit một nấc, tức nó có thể phân ly cho ra một ion H+ và ion clo, Cl−. Khi hòa tan trong nước, H+ liên kết với phân tử nước tạo thành ion hydronium, H3O+:
HCl + H2O → H3O+ + Cl−
Do phân ly hoàn toàn trong nước nên axit clohiđric được xếp vào nhóm axit mạnh.[16][17] Các axit monoproton có một hằng số điện ly, Ka, cho thấy mức độ phân ly của nó trong nước. Đối với các axit mạnh tương tự như HCl, thì Ka có giá trị lớn, và bên cạnh đó, cũng đã có nhiều nghiên cứu lý thuyết để xác định giá trị Ka đối với HCl. Giá trị Ka thường được tính thông qua pKa, giá trị pKa của HCl, tùy theo nguồn, dao động trong khoảng -3 đến -7, thậm chí đến -9,3.
Khi cho các muối clorua như NaCl vào dung dịch HCl thì chúng không ảnh hưởng đến giá trị pH, điều này cho thấy rằng ion Cl− là một gốc bazơ liên hợp cực kỳ yếu và HCl bị phân ly hoàn toàn trong dung dịch. Đối với các dung dịch axit clohiđric trung bình đến mạnh, người ta cho rằng số mol H+ bằng với số mol HCl, với độ tin cậy 4 chữ số thập phân.
Trong số sáu axit vô cơ mạnh phổ biến, axit clohiđric là một axit monoproton ít có khả năng tạo phản ứng giảm số oxy hóa. Nó là một trong những axit mạnh ít độc hại nhất khi tiếp xúc bằng tay; ngoài tính axit, nó còn bao gồm các ion clo không phản ứng và không độc hại. Các dung dịch axit clohiđric trung bình-mạnh thì khá ổn định khi lưu trữ.
Axit clohiđric thường được dùng phổ biến trong việc chuẩn độ dung dịch bazơ. Các axit chuẩn độ mạnh cho các kết quả chính xác hơn do có điểm cuối rõ ràng. Axit clohiđric dạng hỗn hợp đẳng phí (gần 20,2%) có thể được dùng như một tiêu chuẩn cơ bản trong phân tích định lượng, mặc dù nồng độ chính xác của nó phụ thuộc vào áp suất khí quyển khi điều chế nó.
Axit clohiđric thường được dùng trong việc chuẩn bị mẫu trong hóa phân tích. Axit clohiđric đặc có thể hòa tan một số kim loại, tạo ra các khí hydro và clo. Nó phản ứng với các hợp chất bazơ như canxi cacbonat hoặc đồng(II) ôxít, tạo thành các dung dịch hòa tan có thể dùng để phân tích.
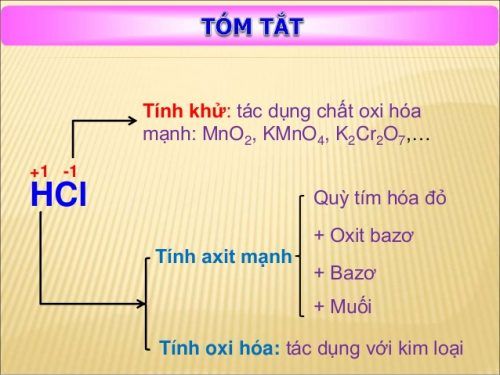
Tương tự các loại axit khác như hclo , hclo3 , hclo4 h2so4, HCl có khả năng tác dụng với:
Kim loại: Giải phóng khí hiđrô và tạo muối clorua (trừ các kim loại đứng sau hiđro trong dãy hoạt động hóa học các kim loại như Cu, Hg, Ag, Pt, Au).
Fe + 2HCl → FeCl2+ H2
Ôxít bazơ: Tạo muối clorua và nước.
ZnO + 2HCl → ZnCl2 + H2O
Bazơ: Tạo muối clorua và nước.
NaOH + HCl → NaCl + H2O
Muối: tác dụng với các muối có gốc anion hoạt động yếu hơn tạo muối mới và axit mới.
CaCO3 + 2HCl → CaCl2 + CO2 + H2O
Ngoài ra, trong một số phản ứng HCl còn thể hiện tính khử bằng cách khử một số hợp chất như KMnO4(đặc), MnO2, KClO3 giải phóng khí clo.
2KMnO4(đặc) + 16HCl → 2KCl + 2MnCl2 + 5Cl2 + 8 H2O
MnO2 + 4HCl → MnCl2 + Cl2 + 2H2O
Trên đây là một số thông tin về tính chất hóa học của axit clohydric, phần so sánh hcl với một vài axit khác sẽ được bộ phận biên tập của Hanimex sớm biên soạn trình bày và gửi đến độc giả trong thời gian sớm nhất.
 Công Ty Hóa Chất Hanimex HANIMEX Chemical
Công Ty Hóa Chất Hanimex HANIMEX Chemical