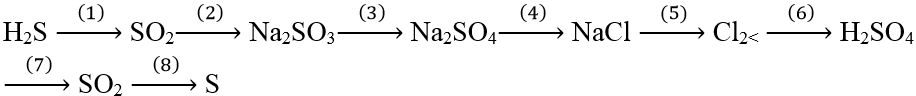Câu 1: Ở nhiệt độ thường
A. O2 không oxi hóa được Ag, O3 oxi hóa được Ag.
B. O2 oxi hóa được Ag, O3 không oxi hóa được Ag.
C. cả O2 và O3 đều không oxi hóa được Ag.
D. cả O2 và O3 đều oxi hóa được Ag.
Đáp án A
Câu 2: Phương trình hóa học nào sau đây sai?
A. KMnO4 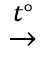
B. 2KClO3 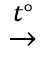
C. 2Ag + O3 → Ag2 O + O2
D. C2 H5 OH + 3O2 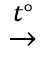
Đáp án A
Câu 3: Cặp chất nào sau đây không tác dụng được với nhau?
A. Ag và O3 B. CO và O2 C. Mg và O2 D. CO2 và O2
Đáp án D
Câu 4: Hơi thủy ngân rất dộc, bởi vậy khi làm vỡ nhiệt kế thủy ngân thì chất bột được dùng để rắc lên thủy ngân rồi gom lại là
A. vôi sống. B. cát. C. muối ăn. D. lưu huỳnh.
Đáp án D
Câu 5: Nguyên tử S đóng vai trò vừa là chất khử, vừa là chất oxi hóa trong phản ứng nào sau đây?
A. 4S + 6NaOH (đặc) 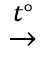
B. S + 3F2 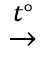
C. S + 6HNO3 (đặc) 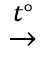
D. S + 2Na 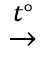
Đáp án A
Câu 6: Trộn sắt bột và lưu huỳnh bột rồi cho vào ống nghiệm khô. Đun ống nghiệm trên ngọn lửa đèn cồn, một lúc sau hỗn hợp cháy đỏ. Sản phẩm tạo thành là
A. sắt(II) sunfua có màu nâu đỏ.
B. sắt(II) sunfua có màu xám đen.
C. sắt(III) sunfua có màu nâu đỏ.
D. sắt(III) sunfua có màu xám đen.
Đáp án B
Câu 7: : Một mẫu khí thải (H2 S, NO2, SO2, CO2) được sục vào dung dịch CuSO4, thấy xuất hiện kết tủa màu đen. Hiện tượng này do chất nào có trong khí thải gây ra?
A. H2 S B. NO2 C. SO2 D. CO2
Đáp án A
Câu 8: Kim loại nào sau đây không tác dụng với dung dịch H2SO4 loãng?
A. Al B. Mg C. Na D. Cu
Đáp án D. Cu
Câu 9: Dung dịch H2SO4 loãng phản ứng được với tất cả các chất trong dãy nào trõng dãy chất nào sau đây?
A. Al2 O3, Ba(OH) 2, Ag
B. CuO, NaCl, CuS
C. FeCl3, MgO, Cu
D. BaCl2, Na2 CO3, FeS
Đáp án D
Câu 10: Thuốc thử nào sau đây dùng để phân biệt khí H2 S với khí CO2?
A. dung dịch HCl
B. dung dịch Pb(NO3) 2
C. dung dịch K2 SO4
D. dung dịch NaCl
Đáp án B
Câu 11: Để phân biệt SO2 và CO2 chỉ cần dùng thuốc thử là
A. dung dịch Ba(OH) 2
B. CaO
C. dung dịch NaOH
D. nước brom
Đáp án D
Câu 12: Để loại bỏ các khí HCl, CO2 và SO2 có lẫn trong khí N2, người ta sử dụng lượng dư dung dịch
A. NaCl B. CuCl2 C. Ca(OH) 2 D. H2SO4
Đáp án C
Câu 13. Chỉ dùng thêm một thuốc thử hãy phân biệt các ung dịch sau: BaCl2, MgSO4, Na2SO3, KNO3, K2S.
Đáp án:
Trích mỗi dung dịch một ít làm mẫu thử
Cho dung dịch H2SO4 lần lượt vào các mẫu thử trên
– Mẫu thử nào tạo kết tủa trắng là BaCl2
BaCl2 + H2SO4 → BaSO4 ↓+ 2HCl
– Mẫu thử nào tạo khí mùi hắc là Na2SO3
Na2SO3 + H2SO4 → Na3SO4+ SO2 ↑+ H2O
– Mẫu thử tạo mùi trứng thối là K2S
K2S + H2SO4 → K2SO4 + H2S↑
Cho dung dịch BaCl2 vừa mới nhận được lần lượt vào hai mẫu thử còn lại:
– Mẫu thử nào tạo kết tủa trắng là MgSO4
BaCl2 + MgSO4 → BaSO4↓ + MgCl2
– Mẫu thử không có hiện tượng gì là KNO3 )
Câu 14. Chỉ dùng nước và một hóa chất khác làm thuỗ thử, hãy phân biệt các chất bột sau: NaCl, CaCO3, Na2S, K2SO3 , Na2SO4
Đáp án:
Cho H2O lần lượt vào các mẫu thử trên
– Mẫu thử không tan trong nước là CaCO3
– Các mẫu thử còn lại ta: NaCl, Na2S, K2SO3, Na2SO4
Cho dung dịch HCl dư lần lượt vào các mẫu thử tan.
– Mẫu thử tạo khí mùi trứng thối là Na2S
Na2S +2 HCl → 2NaCl + H2S↑
– Mẫu thử tạo khí mùi hắc là K2SO3
K2SO3 +2 HCl → 2KCl+ SO2↑+ H2O
– Hai chất không có hiện tượng gì là : NaCl và Na2SO4 (nhóm 1)
Cho dung dịch HCl dư vào chất không tan trong nước, sau đó lây dung dịch vừa thu được lần lượt tác dụng với 2 chất nhóm 1.
– Mẫu thử tạo kết tảu trắng là Na2SO4
CaCl2 + Na2SO4 → CaSO4 + 2NaCl
– Mẫu thử không có hiện tượng gì là NaCl
Câu 15: Cho phương trình hóa học: aS + bH2SO4 (đặc) → cSO2 ↑ + dH2O
Tỉ lệ a:b là
A. 1:1 B. 2:3 C. 1:3 D. 1:2
Đáp án:
Đáp án D
Câu 16: Hoàn thành chuỗi các phản ứng sau, Ghi rõ điều kiện nếu có:
Đáp án:
1) 2H2S + 3O2 dư 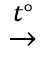
2) SO2 + NaOH → Na2SO3 + H2O
3) 2Na2CO3 + Cl2 + 2H2O → Na2SO4 + 2HCl + H2SO4
4) Na2SO4 + BaCl2 → 2NaCl + BaSO4
5) 2NaCl + 2H2O 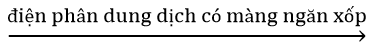
6) Cl2 + SO2 + 2H2O → 2HCl + H2SO4
7) Cu + 2H2SO4 đặc 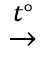
8) 2H22S + SO2 → 3S + 2H2O
Câu 17: Xác định các chất và hoàn thành các phương trình phản ứng sau:
FeS + A → B(khí) + C
B + CuSO4 → D↓đen + E
B + F → G↓vàng + H
C + JKhí → L
L + KI → C + M + N
Đáp án:
A: HCl; B: H2S; C: FeCl2 ; D: CuS ; E: H2SO4; G: S; H: H2O; J: Cl2; L: FeCl3; M:KCl; N: I2
FeS + 2HCl → FeCl2 + H2S↑
H2S + CuSO4 → CuS↓+ H2SO4
2H2S + SO2 → 3S↓ + 2H2O
2FeCl2 +Cl2 → 2FeCl3
FeCl3 + 2KI → 2FeCl2 + 2KCl + I2
Câu 18: KMnO4 → Cl2 → NaClO3 → O2 → SO2 → SO3 → H2SO4
Đáp án:
2KMnO4 + 16HCl 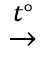
3Cl2+ 6NaOH 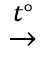
2NaClO3 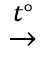
O2 + S 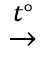
2SO2 + O2 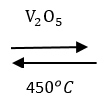
SO3 + H2O → H2SO4
Câu 19: Đốt cháy hoàn toàn 17,4 gam hỗn hợp Mg và Al trong khí oxi (dư) thu được 30,2 gam hỗn hợp oxit. Thể tích khí oxi (đktc) đã tham gia phản ứng là
A. 17,92 lít. B. 8,96 lít. C. 11,20 lít. D. 4,48 lít.
Đáp án:
Đáp án B
Bảo toàn khối lượng: 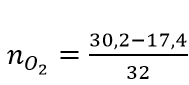
⇒ V = 0,4.22,4 = 8,96 (lít)
Câu 20: Oxi hóa hoàn toàn m gam kim loại X cần vừa đủ 0,25m gam khí O2. X là
A. Al B. Fe C. Cu D. Ca
Đáp án:
Đáp án C
Chọn m = 32 gam ⇒ 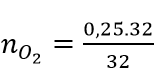
Bảo toàn electron ⇒ 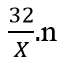
Câu 21: Nhiệt phân hoàn toàn 31,6 gam KMnO4, thu được V lít O2 (đktc). Giá trị của V là
A. 2,24 B. 1,12 C. 4,48 D. 8,96
Đáp án:
Đáp án A
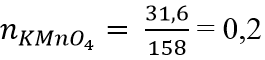
2KMnO4 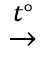
(mol) 0,2 0,1
⇒ V = 0,1.22,4 = 2,24 (lít)
Câu 22: Thêm 3 gam MnO2 vào 197 gam hỗn hợp X gồm KCl và KClO3. Trộn kĩ và đun hỗn hợp đến phản ứng hoàn toàn, thu được chất rắn cân nặng 152 gam. Khối lượng KCl trong 197 gam X là
A. 74,50 gam. B. 13,75 gam. C. 122,50 gam. D. 37,25 gam.
Đáp án:
Đáp án A
Bảo toàn khối lượng:mO2 = 3 + 197 – 152 = 48 (gam)
⇒ 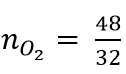
2KClO3 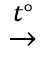
(mol) 1,0 1,5
⇒ mKCl = 197 – 1.122,5 = 74,5 (gam)
Câu 23. Đốt cháy hoàn toàn 12,8 gam lưu huỳnh. Khí sinh ra được hấp thụ hết bởi 150 ml dung dịch NaOH 20% (d= 1,28 g/ml). Tìm CM, C% của các chất trong dung dịch thu được sau phản ứng.
ĐS: Na2SO3 : 2,67 M ; 23,2%. NaOH : 2,67 M ; 7,35%.
Câu 24. Trộn 0,8 mol SO2 với 20,16 lít O2 (đktc) trong bình kín có thể tích không đổi là 100 lít, đun nóng bình đến 400oC, ở nhiệt độ này thấy áp suất trong bình là 0,8 atm. % các chất khí trong bình là:
A. SO2 10%; O2 30%; SO3 60%
B. SO2 15%; O2 70%; SO3 15%
C. SO2 10%; O2 5%; SO3 65%
D. SO2 20,69%; O2 44,83%; SO3 34,48%
Đáp án:
Đáp án D
Chi tiết tại: https://vietjack.com/hoa-hoc-lop-10/bai-tap-hoa-10-chuong-nhom-oxi-luu-huynh.jsp
Tag: dạng bài tập chương violet chuyên đề kiểm tra 10 trắc lý thuyết nâng tóm tắt lớp thi đại loi giai sơ đồ tư duy đốt chiếm 60% về công thức vi khuẩn ôn khó toán thí cơ bản oxi-lưu tự luận
 Công Ty Hóa Chất Hanimex HANIMEX Chemical
Công Ty Hóa Chất Hanimex HANIMEX Chemical