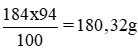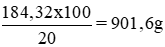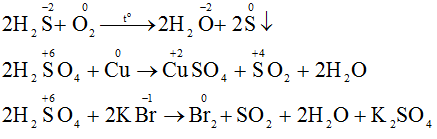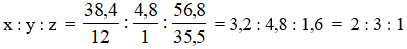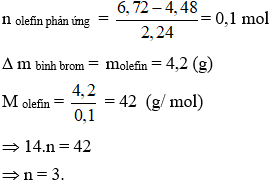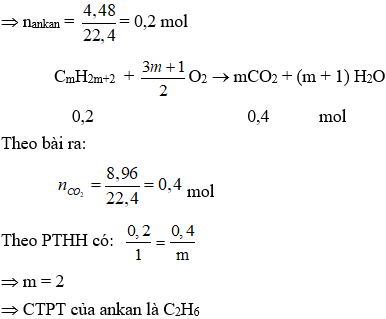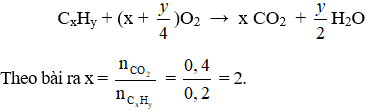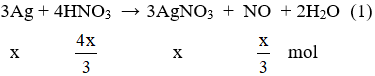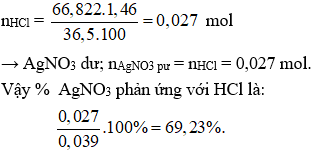Đề Thi – Các Dạng Bài Tập Có Lời Giải Môn Hóa Học Lớp 10
Giải bài tập sgk hóa học lớp 10
Bài 6 (trang 143 SGK Hóa 10): Có 100ml dung dịch H2SO4 98%, khối lượng riêng là 1,84 g/ml. Người ta muốn pha loãng thể tích H2SO4 trên thành dung dịch H2SO4 20%.
a) Tính thể tích nước cần dung để pha loãng.
b) Khi pha loãng phải tiến hành như thế nào?
Lời giải:
a) Thể tích nước cần dùng để pha loãng.
Khối lượng của 100ml dung dịch axit 98%
100ml × 1,84 g/ml = 184g
Khối lượng H2SO4 nguyên chất trong 100ml dung dịch trên:
Khối lượng dung dịch axit 20% có chứa 180,32g H2SO4 nguyên chất:
Khối lượng nước cần bổ sung vào 100ml dung dịch H2SO4 98% để có được dung dịch 20%: 901,6g – 184g = 717,6g
Vì D của nước là 1 g/ml nên thể tích nước cần bổ sung là 717,6 ml.
b)Cách tiến hành khi pha loãng
Khi pha loãng lấy 717,6 ml H2O vào ống đong hình trụ có thể tích khoảng 2 lít. Sau đó cho từ từ 100ml H2SO4 98% vào lượng nước trên, đổ axit chảy theo một đũa thủy tinh, sau khi đổ vài giọt nên dùng đũa thủy tinh khuấy nhẹ đều. Không được đổ nước vào axit 98%, axit sẽ bắn vào da, mắt..và gây bỏng rất nặng
Bài 3 (trang 146 SGK Hóa 10): Khi khí H2S và axit H2SO4 tham gia các phản ứng oxi hóa – khử, người ta có nhận xét:
– Hidro sunfua chỉ thể hiện tính khử.
– Axit sunfuric chỉ thể hiện tính oxi hóa.
a) Hãy giải thích điều nhận xét trên.
b) Đối với mỗi chất, hãy dẫn ra một phản ứng hóa học để minh họa.
Lời giải:
a) Khí H2S và axit sunfuric đặc tham gia các phản ứng oxi hóa – khử thì khí H2S chỉ thể hiện tính khử và H2SO4 đặc chỉ thể hiện tính oxi hóa. Vì trong H2S số oxi hóa của S chỉ có thể tăng, trong H2SO4 số oxi hóa S chỉ có thể giảm.
Vì trong H2S số oxi hóa của S là -2 (là số oxi hóa thấp nhất của S) nên chỉ có thể tăng (chỉ thể hiện tính khử), trong H2SO4 số oxi hóa của S là +6 (là số oxi hóa cao nhất của S) nên chỉ có thể giảm (chỉ thể hiện tính oxi hóa).
b) Phương trình phản ứng hóa học:
Bài 1: Viết bản tường trình (trang 133 SGK Hóa 10)
1. Tính oxi hóa của oxi.
Quan sát hiện tượng
Hiện tượng: Mẩu than cháy hồng.
Khi đưa vào lọ chứa oxi, dây thép cháy trong oxi sáng chói, nhiều hạt nhỏ sáng bắn tóe như pháo hoa.
PTHH: 3Fe + O2 → Fe3O4.
Số oxi hóa của Fe tăng từ 0 đến 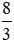
Số oxi hóa của O giảm từ O xuống -2 nên O là chất oxi hóa.
Giải thích hiện tượng: Fe bị oxi hóa trong khí oxi thu được Fe3O4, phản ứng tỏa nhiêt.
2. Sự biến đổi trạng thái của lưu huỳnh theo nhiệt độ.
Tiến hành TN: Lấy 1 lượng nhỏ lưu huỳnh vào ống nghiệm. Đun nóng liên tục ống nghiệm trên ngọn lửa đèn cồn. Quan sát hiện tượng.
Hiện tượng: S(rắn, vàng) → S(lỏng, vàng, linh động) → S(quánh nhớt, nâu đỏ) → S(hơi ,da cam).
Giải thích hiện tượng: S nóng chảy ở 119oC thành chất lỏng màu vàng rất linh động. Ở 187oC lưu huỳnh trở nên quánh nhớt và có màu đỏ nâu. Đến 445oC lưu huỳnh sôi, phân tử S bị phá vỡ thành phân tử nhỏ dạng hơi.
3. Tính oxi hóa của lưu huỳnh.
Tiến hành TN: Cho 1 ít hỗn hợp bột sắt và bột lưu huỳnh vào ống nghiệm
Đun nóng ống nghiệm trên ngọn lửa đèn cồn đến khi thấy có hiện tượng xảy ra phản ứng.
Quan sát hiện tượng
Hiện tượng: Phản ứng giữa Fe và S xảy ra nhanh hơn tỏa nhiều nhiệt, làm đỏ rực hỗn hợp.
PTHH: Fe + S → FeS.
Số oxi hóa của Fe tăng từ 0 → +2 nên Fe là chất khử.
Số oxi hóa của S giảm từ 0 xuống -2 nên S là chất oxi hóa.
Giải thích hiện tượng: Fe bị oxi hóa bởi S tạo FeS, phản ứng tỏa nhiệt.
4. Tính khử của lưu huỳnh.
Tiến hành TN:
Đốt lưu huỳnh trong không khí rồi đưa vào bình chứa khí oxi
Quan sát hiện tượng.
Hiện tượng: S cháy trong lọ chứa O2 mãnh liệt hơn nhiều khi cháy trong không khí, tạo ra khí SO2 có mùi hắc.
PTHH: S + O2 → SO2.
Số oxi hóa của S tăng từ 0 → +4 nên S là chất khử.
Số oxi hóa của O giảm từ 0 xuống -2 nên O là chất oxi hóa.
Giải thích hiện tượng: S bị oxi hóa bởi O2 tạo SO2 có mùi hắc.
Đề tuyển sinh vào lớp 10 Chuyên hóa
Môn thi: Hóa học
Thời gian làm bài: 120 phút
Câu 1. (2 điểm)
1.
a/ Chất nào dùng để khắc chữ và hình trên vật liệu thủy tinh?
b/ Trước khi tiêm, thầy thuốc thường dùng bông tẩm cồn 75° xoa lên da bệnh nhân để sát trùng chỗ tiêm. Tại sao vậy?
2. “Nước đá khô” được sử dụng rộng rãi để bảo quản thực phẩm và một số loại chất kị ẩm. Giải thích tại sao?
Câu 2. (2 điểm)
1. Nêu hiện tượng và viết các Phương trình hóa học xảy ra trong các trường hợp sau:
a/ Dẫn từ từ khí CO2 đến dư vào dung dịch nước vôi trong.
b/ Nhỏ vài giọt dung dịch NaOH vào ống nghiệm chứa 1ml CuSO4. Lắc nhẹ ống nghiệm.
2. Nêu cách pha loãng H2SO4 đặc một cách an toàn. Giải thích.
Câu 3. (2 điểm)
1. Hỗn hợp A gồm Al2O3; MgO; Fe3O4; CuO. Cho luồng H2 dư qua A nung nóng được chất rắn B. Hòa tan B vào dung dịch NaOH dư thu được dung dịch C và chất rắn D. Sục khí CO2 dư vào dung dịch C và hòa tan D bằng dung dịch HNO3 loãng dư (chỉ có duy nhất khí NO bay ra). VIết các phương trình hóa học xảy ra.
2. Muối NaCl bị lẫn các tạp chất NaI; MgCl2; CaCl2; NaBr. Trình bày phương pháp hóa học để thu được NaCl nguyên chất.
Câu 4. (3 điểm)
1. Polime X chứa 38,4% cacbon; 56,8% clo và còn lại là hiđro về khối lượng. Xác định công thức phân tử, viết công thức cấu tạo của X và gọi tên, cho biết trong thực tế X dùng để làm gì?
2. Cho 6,72 lít hỗn hợp khí gồm một ankan và một olefin đi qua dung dịch brom thấy khối lượng bình brom tăng 4,2 gam và thoát ra 4,48 lít khí. Đốt cháy khí thoát ra thu được 8,96 lít khí CO2. Xác định công thức phân tử của các hiđrocacbon, biết thể tích các khí đo ở đktc.
Câu 5. (1 điểm)
Hoà tan hoàn toàn một miếng bạc kim loại vào một lượng dư dung dịch HNO3 15,75% thu được khí NO duy nhất và a gam dung dịch X; trong đó nồng độ C% của AgNO3 bằng nồng độ C% của HNO3 dư. Thêm a gam dung dịch HCl 1,46% vào dung dịch X. Hãy xác định phần trăm khối lượng AgNO3 tác dụng với HCl.
Đáp án & Thang điểm
Câu 1.
1.
a/ Axit flohiđric (HF) hòa tan dễ dàng silic đioxit (SiO2) theo phản ứng sau:
4HF (dd) + SiO2 (r) → SiF4 (k) + 2H2O
Nhờ tính chất này nên HF được dùng để khắc chữ hoặc các họa tiết trên thủy tinh. Do đó, chúng ta có thể trang trí trên thủy tinh như ý muốn.
b/ Vì cồn có khả năng thẩm thấu cao nên có thể thấm sâu vào trong tế bào vi khuẩn, gây đông tụ protein làm cho vi khuẩn chết. Tuy nhiên ở nồng độ cao sẽ làm protein trên bề mặt của vi khuẩn đông tụ nhanh tạo ra lớp màng ngăn không cho cồn thấm sâu vào bên trong, làm giảm tác dụng diệt khuẩn. Ở nồng độ thấp, khả năng động tụ protein giảm, vì vậy hiệu quả sát trùng kém. Thực nghiệm cho thấy cồn 75° có tác dụng diệt khuẩn mạnh nhất.
2.
“Nước đá khô” là CO2 ở trạng thái rắn.
Vì cacbon đioxit ở dạng rắn không nóng chảy mà thăng hoa, khi thăng hoa thu nhiệt rất lớn, làm hạ nhiệt độ của môi trường xung quanh nên tạo môi trường lạnh.
Mặt khác khi đá khô “thăng hoa” sẽ trở thành khí CO2 để bao bọc lấy thực phẩm (tạo môi trường không tồn tại sự sống quanh thực phẩm), tránh vi khuẩn, nấm mốc xâm nhập và làm hỏng thực phẩm, giúp cho thực phẩm giữ được độ tươi ngon và bảo quản được lâu.
Câu 2.
1.
a/ Hiện tượng: Xuất hiện kết tủa trắng, sau đó kết tủa tan khi CO2 dư.
Phương trình hóa học:
CO2 + Ca(OH)2 → CaCO3 (↓ trắng) + H2O
CaCO3 ↓ + CO2 dư + H2O → Ca(HCO3)2
b/ Hiện tượng: Xuất hiện kết tủa xanh lơ lửng trong dung dịch
Phương trình hóa học:
CuSO4 + 2NaOH → Na2SO4 + Cu(OH)2 (↓ xanh)
2. H2SO4 tan vô hạn trong nước và tỏa rất nhiều nhiệt. Nếu ta rót nước vào H2SO4 đặc nước sẽ sôi đột ngột kéo theo những giọt axit bắn ra xung quanh gây nguy hiểm.
Vì vậy, muốn pha loãng axit sunfuric đặc, người ta phải rót từ từ axit vào nước và khuấy nhẹ bằng đũa thủy tinh và tuyệt đối không được làm ngược lại.
Câu 3.
1. Các phương trình hóa học xảy ra:
– Cho H2 dư qua A nung nóng có phản ứng:
Fe3O4 + 4H2 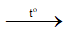
CuO + H2 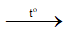
Chất rắn B gồm: Fe; Cu; Al2O3 và MgO.
– Hòa tan B bằng NaOH dư có phản ứng:
Al2O3 + 2NaOH → 2NaAlO2 + H2O
Dung dịch C gồm NaAlO2 và NaOH dư. Sục khí CO2 tới dư vào dung dịch C có các phản ứng:
CO2 + 2H2O + NaAlO2 → Al(OH)3 ↓ + NaHCO3
CO2 + 2NaOH → Na2CO3 + H2O
CO2 dư + Na2CO3 + H2O → 2NaHCO3
Chất rắn D gồm: Fe, Cu, MgO. Cho D tác dụng với HNO3 loãng dư có các phản ứng:
MgO + 2HNO3→ Mg(NO3)2 + H2O
Fe + 4HNO3 → Fe(NO3)3 + NO + 2H2O
3Cu + 8HNO3 → 3Cu(NO3)2 + 2NO + 4H2O
2. Hòa tan hoàn toàn hỗn hợp các muối vào nước thu được dung dich.
Thêm một lượng dư Na2CO3 khi đó sẽ tách được Mg; Ca ra khỏi muối dưới dạng kết tủa:
MgCl2 + Na2CO3 → MgCO3↓ + 2NaCl
CaCl2 + Na2CO3 → CaCO3↓ + 2NaCl
Phần nước lọc còn lại gồm NaCl; NaBr; NaI. Sục khí Clo tới dư vào nước lọc và cô cạn dung dịch sẽ thu được NaCl nguyên chất.
2NaBr + Cl2→ 2NaCl + Br2
2NaI + Cl2 → 2NaCl + I2
Câu 4.
1. Đặt CTTQ của X : CxHyClz
Ta có: %H = 100% – (38,4% + 56,8%) = 4,8%
Ta có tỷ lệ:
Vì X là polime nên công thức phân tử X: (C2H3Cl)n
CTCT X: 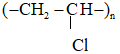
Trong thực tế PVC được dùng làm vật liệu cách điện, ống dẫn nước, vải che mưa …
2.
Đặt CTPT của ankan là CmH2m+2 (m ≥ 1)
Đặt CTPT của olefin là CnH2n (n ≥ 2)
Khi cho hỗn hợp khí qua dung dịch brom chỉ có olefin tham gia phản ứng
CnH2n + Br2 → CnH2nBr2 (1)
Vậy CTPT của olefin là C3H6.
Khi cho hỗn hợp qua dung dịch brom xảy ra hai trường hợp
Trường hợp 1: Brom dư khi đó khí thoát ra là ankan
Trường hợp 2: Brom thiếu trong phản ứng (1) khi đó khí thoát ra là ankan và olefin dư
Đặt CTPT chung của 2 chất là CxHy
Mà n = 3 > 2 nên m < 2 ⇒ m = 1. Vậy CTPT của ankan là CH4.
Vậy CTPT của các hiđrocacbon là CH4 và C3H6 hoặc C2H6 và C3H6.
Câu 5.
* Giả sử có 63 gam dd HNO3 → nHNO3 = 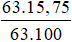
Đặt nAg phản ứng là x mol
Khối lượng dung dịch sau phản ứng = 63 + 108x – 30.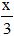
* Do C% (HNO3 dư) = C% (AgNO3) trong dd X nên:
→ x = 0,039 (mol); a = 66,822 gam.
Thêm HCl vào dung dịch X:
HCl + AgNO3 → AgCl ↓ + HNO3 (2)
tag bt nâng kiểm tra chương kì tối ưu windows 25 trắc violet tốt sách giáo khoa cân cương ôn 23 26 lý thuyết amsterdam 33 tổng kiến giỏi chuỗi 7 14 teamviewer 100 việt hsg 32 halogen tốc tự luận 17 cơ 12 ion gì lê phong thông tư đơn bồi dưỡng tóm tắt gta full co dap hướng phát triển lực cấp 21 34 hk2 nhóm 101 triệu chuyển khoản tài sơ đồ phối 13 olympic tphcm 2016 loigiaihay 22 pdf vietjack máy in epson lq 310 tải pes 2010 tỉnh đồng vị online hk1 biểu mũi thư mục tin 11 hà nội quy mua sắm hàng cuộc ngày top cổ phiếu vốn sàn chứng khoán nam soạn lop 24 giai gõ word 400 lần luyện kt trọng tâm office 10-11-12 mẫu bảng kê mới giảng vạn hỏi
 Công Ty Hóa Chất Hanimex HANIMEX Chemical
Công Ty Hóa Chất Hanimex HANIMEX Chemical