Oxit là gì?
– Định nghĩa: Oxit là hợp chất của hai nguyên tố, trong đó có một nguyên tố là Oxi.
Ví dụ: FeO, CuO, SO2, P2O5,..
Cách gọi tên oxit axit
Tên oxit axit: (Tên tiền tố chỉ số nguyên tử của phi kim) + Tên phi kim + (tên tiền tố chỉ số nguyên tử oxi) + ‘‘Oxit’’
| Chỉ số | Tên tiền tố | Ví dụ |
| 1 | Mono (không cần đọc đối với các hợp chất thông thường) | ZnO: Kẽm oxit |
| 2 | Đi
|
UO2: Urani đioxit |
| 3 | Tri | SO3: Lưu huỳnh trioxit |
| 4 | Tetra | |
| 5 | Penta | N2O5: Đinitơ pentaoxit |
| 6 | Hexa | |
| 7 | Hepa | Mn2O7: Đimangan heptaoxit |
Phân loại Oxit
– Để phân loại oxit người ta dựa vào tính chất hóa học của chúng với nước, axit, bazơ,…
– Các Oxit được chia thành 4 loại :
+ Oxit bazơ: Là những oxit khi tác dụng với dung dịch axit, tạo thành muối và nước.
Ví dụ: Na2O, CuO, BaO, FeO,…
+ Oxit axit: Là những oxit khi tác dụng với dung dịch bazơ, tạo thành muối và nước.
Ví dụ: SO2, SO3, CO2, P2O5,…
+ Oxit lưỡng tính: Là những oxit khi tác dụng với dung dịch bazơ, và khi tác dụng với dung dịch axit tạo thành muối và nước.
Ví dụ: Al2O3, ZnO,…
+ Oxit trung tính: Còn được gọi là oxit không tạo muối, là những oxit không tác dụng với axit, bazơ, nước.
Ví dụ: CO, NO,…
Tính chất hóa học của oxit axit
1. Tính tan
Trừ SiO2 thì hầu hết các oxit axit đều tan trong nước để tạo thành dung dịch axit.
Ví dụ:
SO3 + H2O → H2SO4
P2O5 + 3H2O → 2H3PO4
N2O5 + H2O → 2HNO3
SO2 + H2O→ H2SO3
2. Tác dụng với oxit bazo tan để tạo ra muối
Thông thường đó là các oxit tác dụng được với nước (Na2O, CaO, K2O, BaO)
SO3 + CaO -> CaSO4
P2O5 + 3Na2O -> 2Na3PO4
3. Tác dụng với bazơ tan
Bazo tan là bazo của kim loại kiềm và kiềm thổ mới. Cụ thể, có 4 bazo tan như sau: NaOH, Ca(OH)2, KOH, Ba(OH)2.
P2O5 + 6KOH → 2K3PO4 + 3H2O
Tuỳ vào tỉ lệ mol giữa oxit axit và bazơ tham gia phản ứng mà sản phẩm tạo ra sẽ khác nhau, có thể là nước + muối trung hoà, muối axit hoặc hỗn hợp 2 muối.
Gốc axit tương ứng có hoá trị II
Đối với kim loại trong bazơ có hoá trị I:
Tỉ lệ mol bazo và oxit axit là 1: Phản ứng tạo muối axit
NaOH + SO2→ NaHSO3
Tỉ lệ mol bazo và oxit axit là 2: Phản ứng tạo muối trung hoà
2KOH + SO3 → K2SO3 +H2O
Đối với kim loại trong bazơ có hoá trị II
Tỉ lệ mol bazo và oxit axit là 1: Phản ứng tạo muối trung hoà
CO2 + Ca(OH)2 → CaCO3
Tỉ lệ mol bazo và oxit axit là 2: Phản ứng tạo muối axit
SiO2 + Ba(OH)2 → BaSiO3
Đối với axit có gốc axit hoá trị III
Đối với kim loại có hoá trị I:
Tỉ lệ mol bazo và oxit axit là 6:
P2O5 + 6NaOH → 2Na2HPO4 +H2O
Tỉ lệ mol bazo và oxit axit là 4:
P2O5 + 4NaOH → 2NaH2PO4 +H2O
Tỉ lệ mol bazo và oxit axit là 2:
P2O5 + 2NaOH +H2O → 2NaH2PO4
Các oxit axit thường gặp
- CO2: Cacbon đioxit (H2CO3)
- SO2: Lưu huỳnh đioxit (H2SO3)
- SO3: Lưu huỳnh trioxit (H2SO4)
- N2O3: Đinitơ trioxit (HNO2)
- N2O5: Đinitơ pentaoxit (HNO3)
- P2O3: Điphotpho trioxit (H3PO3)
- P2O5: Điphotpho pentaoxit (H3PO4)
- Cl2O: Điclo oxit (HClO)
- Cl2O3: Điclo trioxit (HClO2)
- Cl2O5: Điclo pentaoxit (HClO3)
- Cl2O7: Điclo heptaoxit (HClO4)
- CrO3: Crôm trioxit (H2Cr2O7 và H2CrO4)
- SiO2: silic đioxit (H2SiO3)
- SeO2: Selen đioxit (H2SeO3)
- SeO3: Selen trioxit (H2SeO4)
- Mn2O7: Đimangan heptaoxit (HMnO4)
- I2O: Điiốt oxit (HIO)
- I2O3: Điiốt trioxit (HIO2)
- I2O5: Điiốt pentaoxit (HIO3)
- I2O7: Điiốt heptaoxit (HIO4)
- Br2O: Đibrôm oxit (HBrO)
- Br2O3: Đibrôm trioxit (HBrO2)
- Br2O5: Đibrôm pentaoxit (HBrO3)
- Br2O7: Đibrôm heptaoxit (HBrO4)
- TeO2: Telua đioxit (H2TeO3)
- F2O: Điflo oxit (HFO)
- UO2: Urani đioxit (H2UO3)
- UO3: Urani trioxit (H2UO4)
- WO3: Wolfram trioxit (H2WO4)
- ZnO: Kẽm oxit (H2ZnO2)
- B2O3: Bo oxit (H3BO3)
Tổng hợp bài tập oxit axit tiêu biểu
Trường hợp 1: Khi các oxit axit (CO2, SO2…) tác dụng với dung dịch kiềm (KOH, NaOH…)
Phương trình hóa học
CO2 + NaOH → NaHCO3 (1)
CO2 + 2NaOH → Na2CO3 + H2O (2)
Cách giải
Bước 1: Xét tỉ lệ mol bazo và oxit axit, giả sử là T
– Nếu T ≤ 1: Sản phẩm thu được là muối axit tức chỉ xảy ra phản ứng (1)
– Nếu 1 < T < 2: Sản phẩm thu được là muối axit và muối trung hòa tức xảy ra đồng thời 2 phản ứng (1) và (2)
– Nếu T ≥ 2: Sản phẩm thu được là muối trung hòa tức chỉ xảy ra phản ứng (2).
Bước 2: Viết phương trình phản ứng và tính toán theo phương trình đó (nếu xảy ra cả 2 phản ứng thì cần đặt ẩn và giải theo hệ phương trình)
Bước 3: Tính toán theo yêu cầu của đề bài đã cho
Trường hợp 2: Khi các oxit axit (CO2, SO2…) tác dụng với dung dịch kiềm thổ (Ca(OH)2, Ba(OH)2…)
Phương trình phản ứng
CO2 + Ca(OH)2 → CaCO3 + H2O (1)
2CO2 + Ca(OH)2 → Ca(HCO3)2 (2)
Cách giải
Bước 1: Xét tỉ lệ
– Nếu T ≤ 1: Sản phẩm thu được là muối trung hòa (xảy ra phản ứng (1))
– Nếu 1 < T < 2: Sản phẩm thu được là muối axit và muối trung hòa (xảy ra phản ứng (1) và (2))
– Nếu T ≥ 2: Sản phẩm thu được là muối axit (xảy ra phản ứng (2)).
Bước 2 và bước 3 tương tự trường hợp 1.
Ví dụ: Sục 6,72 lít khí CO2 trong điều kiện tiêu chuẩn vào 400ml dung dịch NaOH 1M. Tính khối lượng muối tạo thành.
Giải
Ta có: nCO2 = 6,72 x 22,4 = 0,3 (mol)
nNaOH = CM x V = 1 x 0,4 = 0,4 (mol)
Phương trình hóa học
CO2 + 2NaOH → Na2CO3 + H2O (1)
Có: 0,3mol 0,4mol
P/ứ: 0,2<- 0,4 -> 0,2
Theo PTHH (1) ta thấy CO2 dư nên số mol tính theo NaOH tức nNa2CO3 = 0,2 (mol)
nCO2 p/ứ = 0,2 (mol) => nCO2 dư = 0,3 – 0,2 = 0, 1 (mol)
CO2 dư : CO2 + Na2CO3 + H2O → 2NaHCO3 (2)
Có : 0,1mol 0,2mol
P/ứ: : 0,1 -> 0,1 -> 0,2
Theo PTHH (2) ta thấy Na2CO3 dư nên số mol tính theo CO2:
nNaHCO3 = 2nCO2 = 0,1 x 2 = 0,2 (mol)
nNa2CO3 dư = 0,2 – 0,1 = 0,1 (mol)
Dung dịch thu được sau phản ứng gồm 2 muối: Na2CO3 (0,1 mol), NaHCO3 (0,2 mol)
mNa2CO3 = 0,1 x 106 = 10,6 (g)
mNaHCO3 = 0,2 x 84 = 16,8 (g)
Bài 1 trang 6 sgk hoá 9: Có những oxit sau: CaO, Fe2O3, SO3. Oxit nào có thể tác dụng được với:
a) Nước.
b) Axit clohiđric.
c) Natri hiđroxit.
Viết các phương trình phản ứng.
* Lời giải bài 1 trang 6 sgk hoá 9:
a) Những oxit tác dụng với nước:
CaO + H2O → Ca(OH)2
SO3 + H2O → H2SO4
b) Những oxit tác dụng với axit clohiđric:
CaO + 2HCl → CaCl2 + H2O
Fe2O3 + 6HCl → 2FeCl3 + 3H2O
c) Những oxit tác dụng với dung dịch natri hiđroxit:
SO3 + NaOH → NaHSO4
SO3 + 2NaOH → Na2SO4 + H2O.
Bài 2 trang 6 sgk hoá 9: Có những chất sau: H2O, KOH, K2O, CO2. Hãy cho biết những cặp chất nào có thể tác dụng với nhau.
* Lời giải bài 2 trang 6 sgk hoá 9:
Những cặp chất tác dụng với nhau từng đôi một:
H2O + CO2 → H2CO3
H2O + K2O → 2KOH
2KOH + CO2 → K2CO3 + H2O
KOH + CO2 → KHCO3
K2O + CO2 → K2CO3
Bài 3 trang 6 sgk hoá 9: Từ những chất sau: Canxi oxit, lưu huỳnh đioxit, cacbon đioxit, lưu huỳnh trioxit, kẽm oxit, em hãy chọn một chất thích hợp điền vào các phản ứng:
a) Axit sunfuric + … → kẽm sunfat + nước
b) Natri hiđroxit + … → natri sunfat + nước
c) Nước + … → axit sunfurơ
d) Nước + … → canxi hiđroxit
e) Canxi oxit + … → canxi cacbonat
Dùng các công thức hóa học để viết tất cả những phương trình phản ứng hóa học trên.
* Lời giải bài 3 trang 6 sgk hoá 9:
a) H2SO4 + ZnO → ZnSO4 + H2O
b) 2NaOH + SO3 → Na2SO4 + H2O
c) H2O + SO2 → H2SO3
d) H2O + CaO → Ca(OH)2
e) CaO + CO2 → CaCO3
Bài 4 trang 6 sgk hoá 9: Cho những oxit sau: CO2, SO2, Na2O, CaO, CuO. Hãy chọn những chất đã cho tác dụng với:
a) nước để tạo thành axit.
b) nước để tạo thành dung dịch bazơ.
c) dung dịch axit để tạo thành muối và nước.
d) dung dịch bazơ để tạo thành muối và nước.
Viết các phương trình phản ứng hóa học trên.
* Lời giải bài 4 trang 6 sgk hoá 9:
a) CO2, SO2 tác dụng với nước tạo thành axit:
CO2 + H2O → H2CO3
SO2 + H2O → H2SO3
b) Na2O, CaO tác dụng với nước tạo thành dung dịch bazơ:
Na2O + H2O → 2NaOH
CaO + H2O → Ca(OH)2
c) Na2O, CaO, CuO tác dụng với axit tạo thành muối và nước:
Na2O + 2HCl → 2NaCl + H2O
CaO + H2SO4 → CaSO4 + H2O
CuO + H2SO4 → CuSO4 + H2O
d) CO2, SO2 tác dụng với dung dịch bazơ tạo thành muối và nước:
CO2 + 2NaOH → Na2CO3 + H2O
SO2 + 2NaOH → Na2SO3 + H2O
Bài 5 trang 6 sgk hoá 9: Có hỗn hợp khí CO2 và O2. Làm thế nào có thể thu được khí O2 từ hỗn hợp trên? Trình bày cách làm và viết phương trình phản ứng hóa học.
* Lời giải bài 5 trang 6 sgk hoá 9:
Dẫn hỗn hợp khí CO2 và O2 đi qua bình đựng dung dịch kiềm (dư) (Ca(OH)2, NaOH…) khí CO2 bị giữ lại trong bình, do có phản ứng sau:
CO2 + Ca(OH)2 → CaCO3↓ + H2O
Hoặc CO2 + 2NaOH → Na2CO3 + H2O
Bài 6 trang 6 sgk hoá 9: Cho 1,6g đồng (II) oxit tác dụng với 100g dung dịch axit sunfuric có nồng độ 20%.
a) Viết phương trình phản ứng hóa học.
b) Tính nồng độ phần trăm các chất có trong dung dịch sau khi phản ứng kết thúc.
* Lời giải bài 6 trang 6 sgk hoá 9:
– Theo bài ra, cho 1,6g đồng (II) oxit tác dụng với 100g dung dịch axit sunfuric nên ta có:
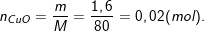
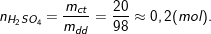
a) Phương trình hoá học của phản ứng:
CuO + H2SO4 → CuSO4 + H2O
b) Theo phương trình phản ứng trên thì lượng CuO tham gia phản ứng hết, H2SO4 còn dư.
– Nên khối lượng CuSO4 tạo thành được tính theo số mol CuO:
nCuSO4 = nCuO = 0,02 (mol) ⇒ mCuSO4 = 0,02.160 = 3,2 (g).
– Khối lượng H2SO4 dư sau phản ứng là:
mH2SO4 = 20 – 98.0,02= 18,04 (g).
– Nồng độ phần trăm của các chất trong dung dịch sau phản ứng là:
C%(CuSO4) =  .100% = 3,15%
.100% = 3,15%
C%(H2SO4) = 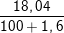 .100% = 17,76%
.100% = 17,76%
Tag: luyện hcl dưới đây lưỡng hay chứng minh thuộc phải oxit+oxit- co cro3 quát sắt từ clohidric td vs vừa nhận xác chuyên ôxit bảng gì dd cộng cr crom igf g h20 h2 hút ẩm khái niệm mạnh phòng thí nghiệm chế trực tiếp n2 nghĩa p sao tac vd ở cro đúng sai 9 photphoric bari hidroxit kali dạng dãy (hcl) đặc nóng phát tại al2o3 bai tap ve voi dich về dấu hiệu la j kể lấy lý thuyết liệt kê mgo mno2 mn2o7 nêu quan trọng sio2 tuong ung cthh yếu kiểm tra tiết ôn thực hành lớp violet tìm muoi dinh nghia va nhan biet
 Công Ty Hóa Chất Hanimex HANIMEX Chemical
Công Ty Hóa Chất Hanimex HANIMEX Chemical