Tính Chất Hóa Học Của Các Loại Hợp Chất Phổ Biến Chứa Sắt
Sắt là tên một nguyên tố hóa học trong bảng tuần hoàn nguyên tố có ký hiệu Fe và số hiệu nguyên tử bằng 26. Nằm ở phân nhóm VIIIB chu kỳ 4. Sắt và Niken (Ni) được biết là 2 nguyên tố cuối cùng có thể tạo thành qua tổng hợp ở nhân sao (hình thành qua phản ứng hạt nhân ở tâm các vì sao) mà không cần phải qua một vụ nổ siêu tân tinh hay các biến động lớn khác. Do đó sắt và Niken khá dồi dào trong các thiên thạch kim loại và các hành tinh lõi đá (như Trái Đất, Sao Hoả)
Một nguyên tử sắt điển hình có khối lượng gấp 56 lần khối lượng một nguyên tử hiđrô điển hình. Sắt là kim loại phổ biến nhất, và người ta cho rằng nó là nguyên tố phổ biến thứ 10 trong vũ trụ. Sắt cũng là nguyên tố phổ biến nhất (theo khối lượng, 34.6%) tạo ra Trái Đất; sự tập trung của sắt trong các lớp khác nhau của Trái Đất dao động từ rất cao ở lõi bên trong tới khoảng 5% ở lớp vỏ bên ngoài; có thể phần lõi của Trái Đất chứa các tinh thể sắt mặc dù nhiều khả năng là hỗn hợp của sắt và niken; một khối lượng lớn của sắt trong Trái Đất được coi là tạo ra từ trường của nó. Ký hiệu của sắt Fe là từ viết tắt của ferrum, từ Latinh của sắt.
I. Hợp chất của sắt II – Fe (II)
– Trong các phản ứng hoá học ion Fe2+ dễ nhường 1e để trở thành ion Fe3+
Fe2+ + 1e → Fe3+
– Như vậy tính chất đặc trưng của hợp chất sắt 2 – Fe (II) là tính khử
1. Tính chất hoá học của Sắt (II) oxit – FeO
– Là chất rắn, đen, không tan trong nước.
– Tính chất hoá học:
+ FeO là oxit bazơ:
– FeO tác dụng với axit HCl: Fe + HCl
FeO + 2HCl → FeCl2 + H2↑
– FeO tác dụng với axit H2SO4: Fe + H2SO4
FeO + H2SO4 loãng → FeSO4 + H2O
+ FeO là chất oxi hóa khi tác dụng với các chất khử mạnh: H2, CO, Al → Fe:
– FeO tác dụng với H2: FeO + H2
FeO + H2 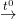 Fe + H2O
Fe + H2O
– FeO tác dụng với CO: FeO + CO
FeO + CO 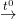 Fe + CO2
Fe + CO2
3FeO + 2Al 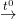 Al2O3 + 3Fe
Al2O3 + 3Fe
+ FeO là chất khử khi tác dụng với các chất có tính oxi hóa mạnh:
– FeO tác dụng với O2: FeO + O2
FeO + O2 → 2Fe2O3
– FeO tác dụng với axit HNO3: FeO + HNO3
3FeO + 10HNO3 loãng → 3Fe(NO3)3 + NO + 5H2O
– Điều chế FeO:
FeCO3 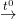 FeO + CO2 (nung trong điều kiện không có không khí)
FeO + CO2 (nung trong điều kiện không có không khí)
Fe(OH)2 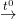 FeO + H2O (nung trong điều kiện không có không khí)
FeO + H2O (nung trong điều kiện không có không khí)
2. Oxit sắt từ Fe3O4 (FeO.Fe2O3)
– Là chất rắn, đen, không tan trong nước và có từ tính.
– Tính chất hoá học:
+ Fe3O4 là oxit bazơ:
– Fe3O4 tác dụng với axit HCl: Fe3O4 + HCl
Fe3O4 + 8HCl → 2FeCl3 + FeCl2 + 4H2O
– Fe3O4 tác dụng với axit HCl: Fe3O4 + H2SO4
Fe3O4 + 4H2SO4 loãng → Fe2(SO4)3 + FeSO4 + 4H2O
+ Fe3O4 là chất khử: Fe3O4 + HNO3
3Fe3O4 + 28HNO3 → 9Fe(NO3)3 + NO↑+ 14H2O
+ Fe3O4 là chất oxi hóa:
– Fe3O4 tác dụng với H2: Fe3O4 + H2
Fe3O4 + 4H2 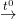 3Fe + 4H2O
3Fe + 4H2O
– Fe3O4 tác dụng với CO: Fe3O4 + CO
Fe3O4 + 4CO 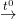 3Fe + 4CO2
3Fe + 4CO2
– Fe3O4 tác dụng với Al: Fe3O4 + Al
3Fe3O4 + 8Al 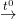 4Al2O3 + 9Fe
4Al2O3 + 9Fe
– Điều chế: thành phần quặng manhetit
3Fe + 2O2 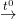 Fe3O4
Fe3O4
3Fe + 4H2O ![small xrightarrow[]{<570^{0}C}](https://hayhochoi.vn/uploads/news/wyswyg/2019_02/giflatexsmallspacexrightarrow570_1550485394.gif) Fe3O4 + 4H2↑
Fe3O4 + 4H2↑
3. Sắt (II) hidroxit Fe(OH)2
– Là chất kết tủa màu trắng xanh.
– Fe(OH)2 là bazơ không tan:
+ Fe(OH)2 Bị nhiệt phân:
Fe(OH)2 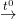 FeO + H2O (nung trong điều kiện không có không khí)
FeO + H2O (nung trong điều kiện không có không khí)
4Fe(OH)2 + O2 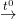 2Fe2O3 + 4H2O (nung trong không khí)
2Fe2O3 + 4H2O (nung trong không khí)
+ Tan trong axit không có tính oxi hóa → muối sắt (II) và nước:
– Fe(OH)2 tác dụng với HCl: Fe(OH)2 + HCl
Fe(OH)2 + 2HCl → FeCl2 + 2H2O
+ Có tính khử (do Fe có mức oxi hóa +2):
– Fe(OH)2 tác dụng với O2: Fe(OH)2 + O2
4Fe(OH)2 + O2 + 2H2O → 4Fe(OH)3
– Fe(OH)2 tác dụng với O2: Fe(OH)2 + HNO3
3Fe(OH)2 + 10HNO3 loãng → 3Fe(NO3)3 + NO + 8H2O
– Điều chế Fe(OH)2 :
Fe2+ + 2OH– → Fe(OH)2 (trong điều kiện không có không khí)
4. Muối sắt II
-Không bền, có tính khử, khi tác dụng với chất oxi hóa tạo thành muối sắt (III).
2FeCl2 + Cl2 → 2FeCl3
3Fe(NO3)2 + 4HNO3 → 3Fe(NO3)3 + NO + 2H2O
2FeSO4 + 2H2SO4 đặc nóng → Fe2(SO4)3 + SO2 + 2H2O
10FeSO4 + 2KMnO4 + 8H2SO4 → 5Fe2(SO4)3 + K2SO4 + 2MnSO4 + 8H2O
6FeSO4 + K2Cr2O7 + 7H2SO4 → 3Fe2(SO4)3 + K2SO4 + Cr2(SO4)3 + 7H2O
* Chú ý: Các muối sắt (II) không tan như FeCO3, FeS, FeS2 bị đốt nóng trong không khí tạo Fe2O3.
2FeCO3 + ½O2 → Fe2O3 + 2CO2
4FeS + 9O2 → 2Fe2O3 + 4SO2
4FeS2 + 11O2 → 2Fe2O3 + 8SO2
II. Hợp chất của sắt III – Fe (III)
– Trong các phản ứng hoá học ion Fe3+ có khả năng nhận 1e đến 3e để trở thành ion Fe2+ hoặc Fe:
Fe3+ + 1e → Fe2+
Fe3+ + 3e → Fe
– Như vậy tính chất đặc trưng của hợp chất sắt 3 – Fe (III) là tính oxi hóa.
1. Tính chất hoá học của Sắt (III) oxit – Fe2O3
– Là chất rắn, nâu đỏ, không tan trong nước.
– Tính chất hoá học:
+ Là oxit bazơ:
– Fe2O3 tác dụng với HCl: Fe2O3 + HCl
Fe2O3 + 6HCl → 2FeCl3 + 3H2O
– Fe2O3 tác dụng với H2SO4 : Fe2O3 + H2SO4
Fe2O3 + 3H2SO4 → Fe2(SO4)3 + 3H2O
– Fe2O3 tác dụng với H2SO4 : Fe2O3 + HNO3
Fe2O3 + 6HNO3 → 2Fe(NO3)3 + 3H2O
+ Là chất oxi hóa:
– Fe2O3 tác dụng với H2 : Fe2O3 + H2
Fe2O3 + 3H2 ![small xrightarrow[]{t^{0}}](https://hayhochoi.vn/uploads/news/wyswyg/2019_02/giflatexsmallspacexrightarrowt_1550488256.gif) 2Fe + 3H2O
2Fe + 3H2O
– Fe2O3 tác dụng với CO : Fe2O3 + CO
Fe2O3 + 3CO ![small xrightarrow[]{t^{0}}](https://hayhochoi.vn/uploads/news/wyswyg/2019_02/giflatexsmallspacexrightarrowt_1550488256.gif) 2Fe + 3CO2
2Fe + 3CO2
– Fe2O3 tác dụng với Al : Fe2O3 + Al
Fe2O3 + 2Al ![small xrightarrow[]{t^{0}}](https://hayhochoi.vn/uploads/news/wyswyg/2019_02/giflatexsmallspacexrightarrowt_1550488256.gif) Al2O3 + 2Fe
Al2O3 + 2Fe
– Điều chế: thành phần của quặng hematit
2Fe(OH)3 ![small xrightarrow[]{t^{0}}](https://hayhochoi.vn/uploads/news/wyswyg/2019_02/giflatexsmallspacexrightarrowt_1550488256.gif) Fe2O3 + 3H2O
Fe2O3 + 3H2O
2. Sắt (III) hidroxit Fe(OH)3
– Là chất kết tủa màu nâu đỏ.
– Tính chất hoá học:
+ Là bazơ không tan:
+ Bị nhiệt phân:
2Fe(OH)3 → Fe2O3 + 3H2O
+ Tan trong axit → muối sắt (III):
– Fe(OH)3 tác dụng với HCl : Fe(OH)3 + HCl
Fe(OH)3 + 3HCl → FeCl3 + 3H2O
– Fe(OH)3 tác dụng với HNO3 : Fe(OH)3 + HNO3
Fe(OH)3 + 3HNO3 → Fe(NO3)3 + 3H2O
– Điều chế Fe(OH)3:
Fe3+ + 3OH– → Fe(OH)3
3. Muối sắt (III)
– Có tính oxi hóa khi tác dụng với chất khử.
2FeCl3 + Cu → CuCl2 + 2FeCl2
2FeCl3 + 2KI → 2FeCl2 + 2KCl + I2
2FeCl3 + H2S → 2FeCl2 + 2HCl + S
– Các dung dịch muối sắt (III) có môi trường axit:
Fe3+ + 3H2O ↔ Fe(OH)3 + 3H+
– Khi cho muối sắt (III) tác dụng với các kim loại cần lưu ý:
+ Nếu kim loại là Na, Ca, K, Ba + H2O → Kiềm + H2. Kiềm + Fe3+ → Fe(OH)3
+ Nếu kim loại không tan trong nước và đứng trước Fe + Fe3+ → Fe2+ → Fe
+ Nếu kim loại là Cu hoặc Fe + Fe3+ → Fe2+
– Các muối sắt (III) bị thủy phân hoàn toàn trong môi trường kiềm:
2FeCl3 + 3Na2CO3 + 3H2O → 2Fe(OH)3 + 6NaCl + 3CO2
Sắt là kim loại được sử dụng nhiều nhất, chiếm khoảng 95% tổng khối lượng kim loại sản xuất trên toàn thế giới. Sự kết hợp của giá thành thấp và các đặc tính tốt về chịu lực, độ dẻo, độ cứng làm cho nó trở thành không thể thay thế được, đặc biệt trong các ứng dụng như sản xuất ô tô, thân tàu thủy lớn, các bộ khung cho các công trình xây dựng. Thép là hợp kim nổi tiếng nhất của sắt, ngoài ra còn có một số hình thức tồn tại khác của sắt như:
* Gang thô (gang lợn) chứa 4% – 5% cacbon và chứa một loạt các chất khác như lưu huỳnh, silic, phốt pho. Đặc trưng duy nhất của nó: nó là bước trung gian từ quặng sắt sang thép cũng như các loại gang đúc (gang trắng và gang xám).
* Gang đúc chứa 2% – 3.5% cacbon và một lượng nhỏ mangan. Các chất có trong gang thô có ảnh hưởng xấu đến các thuộc tính của vật liệu, như lưu huỳnh và phốt pho chẳng hạn sẽ bị khử đến mức chấp nhận được. Nó có điểm nóng chảy trong khoảng 1420–1470 K, thấp hơn so với cả hai thành phần chính của nó, làm cho nó là sản phẩm đầu tiên bị nóng chảy khi cacbon và sắt được nung nóng cùng nhau. Nó rất rắn, cứng và dễ vỡ. Làm việc với đồ vật bằng gang, thậm chí khi nóng trắng, nó có xu hướng phá vỡ hình dạng của vật.
* Thép carbon chứa từ 0,5% đến 1,5% cacbon, với một lượng nhỏ mangan, lưu huỳnh, phốt pho và silic.
* Sắt non chứa ít hơn 0,5% cacbon. Nó là sản phẩm dai, dễ uốn, không dễ nóng chảy như gang thô. Nó có rất ít cacbon. Nếu mài nó thành lưỡi sắc, nó đánh mất tính chất này rất nhanh.
* Các loại thép hợp kim chứa các lượng khác nhau của cacbon cũng như các kim loại khác, như crôm, vanađi, môlipđen, niken, vonfram, v.v.
* Ôxít sắt (III) được sử dụng để sản xuất các bộ lưu từ tính trong máy tính. Chúng thường được trộn lẫn với các hợp chất khác, và bảo tồn thuộc tính từ trong hỗn hợp này.
Các trạng thái ôxi hóa chung của sắt bao gồm:
* Trạng thái sắt(II), Fe2+, ferrous rất phổ biến.
* Trạng thái sắt(III), Fe3+ ,ferric, cũng rất phổ biến, ví dụ trong gỉ sắt.
* Trạng thái sắt(IV), Fe4+, ferryl, ổn định trong các enzym (ví dụ perôxidas).
* Sắt(VI) cũng được biết tới, nó hiếm hơn, có trong ferrat kali.
* cacbua sắt Fe3C được biết đến như là cementit.
TAGs : 12 tẩy rửa giòn nhuộm thùng đựng những nào sunfat thực đồng crom báo cáo
 Công Ty Hóa Chất Hanimex HANIMEX Chemical
Công Ty Hóa Chất Hanimex HANIMEX Chemical